Актинид
Cтраница 3
У актинидов величина разницы свободной энергии образования различных ионов указывает на заметное комплексообразо-вание этих элементов в растворах. Промежуточные степени окисления неустойчивы по отношению к взаимному окислению и восстановлению, и равновесная смесь может поэтому состоять из трех и даже четырех степеней окисления. [31]
Разделение актинидов и очистка их от продуктов деления при помощи экстракции органическими растворителями является ярким примером решения очень сложной задачи разделения смеси элементов, принадлежащих к различным группам периодической системы элементов. Успех разделения такой смеси обеспечивается тончайшим подбором физико-химических условий проведения технологического процесса разделения. [32]
Тетрафториды актинидов имеют структурный тип ZrF4, в котором атом металла окружен 8F по углам тетрагональной антипризмы. Таким образом, средняя длина связи U-F равна 2 28 А. [33]
Ионы актинидов с более высокой валентностью изучены в соединениях, в основном отличных от тех, которые характерны для 4 / - группы. В двух группах наиболее важных из этих соединений ионы актинидов расположены в узлах решетки с симметрией правильного октаэдра. В газовой фазе структура молекул UF6, NpF6 и PuF6 такова, что атом металла находится в центре правильного октаэдра, образованного шестью атомами фтора, которые отстоят от атома металла на расстояниях 0 1996, 0 1981 и 0 1971 нм соответственно. Некоторые из четырехвалентных ионов были исследованы в соединениях Cs2ZrCle и [ ( CH3) 4N ] 2PtCl6, в каждом из которых ион металла окружен правильным октаэдром из ионов хлора. [34]
Спектры актинидов ( интраконфигурационные) / - Ю 4 для переходов, разрешенных по спину, и / - 10 - 5 - 10 - 6 для переходов, запрещенных по спину. [35]
Для актинидов в состоянии окисления ( VI) чрезвычайно характерна конфигурация комплекса в виде гексагональной бипирамиды. Многие соединения, например Кз № [ 1Ю2 ( СО3) 3 ], Cs [ UO2 ( NO3) 3 ], Na [ UO2 ( CH3COO) 3 ], где карбонатный, нитратный и ацетатный ионы бидентатны, построены по этому типу. [36]
Ионы актинидов, как правило, могут быть удалены со смолы путем вымывания такими ионами, как хлорид, нитрат, сульфат и особенно цитрат, лактат, а-гидрокси-бутират, этилендиаминтетрацетат. Порядок вымывания сорбированных ионов зависит от равновесия между степенью адсорбции на смоле и прочностью комплексных ионов, образуемых с вымывающим агентом. При вымывании с колонки для ионов актинидов и лантанидов часто наблюдается порядок, обратный их порядковым номерам. [37]
Ионы актинидов образуют комплексные ионы с большим числом органических веществ, которые хорошо растворимы в этих веществах. Реакции с такого рода веществами меняются от элемента к элементу и в большой степени зависят от окислительного состояния. Ряд важных процессов разделения, в особенности промышленное выделение плутония, основываются на этом свойстве. Органические растворители, взаимодействующие подобным образом и не смешивающиеся с водой, используются для извлечения плутония из водных растворов. [38]
Для актинидов, как и для большинства других элементов, спектроскопическая идентификация является важным методом анализа. В табл. 11.15 приводится перечень длин волн, соответствующих основным линиям, пригодным для этой цели. [39]
 |
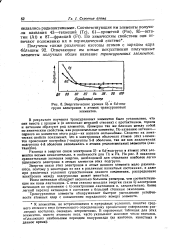
Возрастание устойчивости 5 / - конфигурации по сравнению с бй-конфигурацией в зависимости от повышения заряда иона тория. [40] |
У актинидов Gd-конфигурация более устойчива для нейтрального тория. [41]
Алкоксиды актинидов [93, 94] обладают значительной устойчивостью и относительно высокой летучестью. Хорошо изучены алкоксиды урана. [42]
 |
Энергетические уровни 5 / - и Gd-под. [43] |
Ионы актинидов обладают несколько большим размером, чем соответствующие им ионы лантанидов. С этим связана меньшая энергия связи 5 / - электронов актинидов по сравнению с 4 / - электронами лантанидов и, следовательно, более легкий переход актинидов в состояние с большей степенью окисления. [44]
 |
Прибор Баумбаха для быть Удалены из системы без пре-получения гидридов. кращения тока газа с помощью. [45] |
Страницы: 1 2 3 4