Тропановый алкалоид
Cтраница 1
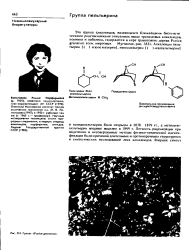
Тропановые алкалоиды обычно встречаются в природных источниках в виде эфиров троповой [ как в соединении ( 15) ] или тигли-новой [ как в соединении ( 23) ] кислот. В троповой кислоте сохранены все девять углеродных атомов фенилаланина; результаты изучения трансформации меченного 14С фенилаланина показывают, что перегруппировка в троповую кислоту осуществляется путем миграции карбоксильной группы от С-2 к С-3. [1]
Природные Тропановые алкалоиды представляют собой производные нортропана с различными заместителями. [2]
Стереоструктура третьего важнейшего тропанового алкалоида ско-поламина все еще не имеет ( подобно его синтезу) таких убедительных экспериментальных доказательств, как в случае рассмотренных выше атропина и кокаина. Однако вполне определенные выводы о стерео-структуре скополамина могут быть сделаны 41 из известных данных о его свойствах ( см. стр. Естественно предположить, что легкость этого превращения связана с тем, что гидроксильная группа при Сз размещена в пространстве близко к оксидному мостику при С6 и С7 что наиболее вероятно в том случае, когда циклогепта-новая система тропанового ядра будет иметь седловидную форму, а пи-перидиновое кольцо - кресловидную. [3]
Тесно связан с тропановыми алкалоидами псевдопельтьерия ( см. стр. [4]
По аналогии с биосинтезом тропановых алкалоидов ( см, разд. Основание ( 82) также образуется из лизина с обычным сохранением индивидуальности атомов С-2 и С-6 аминокислоты. [5]
Важным проявлением генетической связи различных тропановых алкалоидов является также общность их стереоструктуры ( см. стр. [6]
Гиоециамин - наиболее распространенный из тропановых алкалоидов; он очень близко напоминает атропин; главным отличием его физических свойств является оптическая активность [ а ] 0 - - 20 75; он плавится при 108 5 и несколько лучше растворим в воде, чем атропин. Центр оптической асимметрии находится в той части молекулы, которую составляет троповая кислота; следовательно, гиосциамин представляет собой ( -) - тропилтропеин. Гиос-циамин настолько легко рацемизируется, что почти нет сомнения в том, что в природе находится именно эта конфигурация и что в процессе выделения происходит рацемизация с образованием атропина. Вращение его медленно уменьшается при стоянии в растворенном виде ( стр. [7]
В природных условиях сырьевым источником тропановых алкалоидов являются продукты распада углеводов и белков. [8]
Приведенная выше схема связывает воедино все тропановые алкалоиды, включая содержащий эпоксидное кольцо скополамин и производные ди - и триокситрошша - метелоидин и валероидин ( см. стр. [9]
Близость структур гигрина ( 2) и тропановых алкалоидов, например гиосциамина ( 15) и кускогигрина ( 14), позволяет предположить, что гигрин может выполнять роль предшественника этих алкалоидов; это подтверждается описанными выше экспериментами с мечеными соединениями. [10]
Связь между химическим строением и физиологическим действием тропановых алкалоидов представляет много интересных проблем. [11]
Следует отметить, что по общей схеме синтеза тропановых алкалоидов, исходя из глутарового альдегида ( XI), метиламина ( VIII) и бензоил-уксусной кислоты ( XII), получен с 90 % - ным выходом ( 25, рН4, 8 час. [12]
Этот интересный метод был наиболее успешно применен для установления стереохимии тропановых алкалоидов. [13]
Бициклическая система тропана лежит в основе большой группы природных веществ - тропановых алкалоидов. Тропановый цикл может существовать в двух конформациях. В одной из них [ ( 26а) пиперидино-вый цикл имеет форму кресла, в другой [ ( 266) ] - форму ванны, причем в зависимости от природы заместителей более выгодной может оказаться то одна, то другая конформация. [14]
 |
Гранат ( Punica granatum. [15] |
Страницы: 1 2 3