Алкенилбензол
Cтраница 2
 |
Характеристические пики в масс-спектрах ( 70 эВ. [16] |
Как и в алифатических олефиновых углеводородах, двойная связь в алкенилбензолах способна мигрировать под действием ЭУ, Поэтому масс-спектры изомеров в данном ряду качественно сходны, хотя количественные различия порой бывают исключительно велики. [17]
Вероятно, поэтому интенсивность пиков указанных ионов в масс-спектрах изомерных р-метилстиролу алкенилбензолов, отличающихся местом присоединения метальной группы ( а-метилстирол) и положением двойной связи ( аллилбензол), понижена. [18]
Однако двойная связь, сопряженная с ароматическим ядром, обусловливает значительную величину стабильности высших алкенилбензолов по сравнению с изомерными нафте-но-ароматическими углеводородами. Так, для 7-фенил - 6-тридецена WM составляет 14 5 %, тогда как для 2-бутил - 8-гексилтетралина - 3 9 %, Для изомерных алкенилбензолов, отличающихся положением двойной связи и положением метильного заместителя в алке-нильной цепи, - различия в стабильности молекул практически не обнаруживаются. [19]
Определение углеводородных групп: парафиновых, нафтеновых, моноолефиновых, суммарно диеновых и циклоолефиновых, алкил бензолов, алкенилбензолов. Так как моноолефиновые и нафтеновые углеводороды образуют одинаковые характеристические ионы, их определение при совместном присутствии невозможно. Поэтому часть образца обрабатывают концентрированной серной кислотой для удаления олефиновых и ароматических углеводородов и в насыщенной части определяют содержание нафтеновых углеводородов. Непредельные соединения определяются затем по разности. [20]
Влияние фенильного кольца на реакционную способность боковой цепи и характер образующихся продуктов также может быть замечено по результатам щелочной изомеризации некоторых алкенилбензолов. Когда связь С С сопряжена с ароматическим кольцом, то суммарная энергия делокализации выше, чем для случая молекул, в которых эта связь отделена от кольца одной или более СН2 - группой. [21]
Эти реакции идут с увеличением объема и поглощением тепла Соответственно, с повышением температуры и снижением парциального давления углеводородов увеличивается степень превращения алкилбензола в алкенилбензол. [22]
Метод позволяет устанавливать содержание парафиновых углеводородов нормального и изостроения пяти - и шестичленных нафтеновых моноолефиновых цикло - и диолефиновых углеводородов, алкил - и алкенилбензолов. Схема анализа приведена на стр. [23]
Соединения второго типа, которые более правильно называть жир-ноароматическими кремнийорганическими мономерами, могут быть синтезированы металлорганическим методом, кремнеалкилированием ароматических соединений хлоралкилхлорсиланями и присоединением гидридсиланов к алкенилбензолам. Рассмотрение двух первых методов приводится в данной части монографии. Последний метод обсуждается в части IV монографии. [24]
Интенсивности некоторых характеристических полос ( 1000, 1200, 1600 см 1) арилцикланов выше интенсивности соответствующих полос в спектрах алкилбензолов, но ниже, чем у алкенилбензолов. [25]
Разработанная методика позволяет определять в продуктах алкилирования бензола полимерами пропилена или а-олефинами, получающимися от крекинга парафина, следующие группы углеводородов: парафиновые, суммарно нафтеновые и олефиновые, ал-килбензолы и алкенилбензолы. В алкилбензолах анализируются следующие изомеры: 1) моноалкилбензолы, за исключением 2-фенилалканов; 2) 2-фенилалканы; 3) суммарно о - и и-диалкилбен-золы; 4) л-диалкилбензолы. [26]
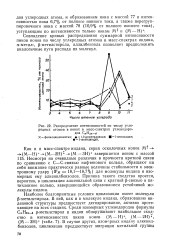 |
Распределение интенсивностей по числу углеродных атомов в ионах в масс-спектрах углеводородов С Н2га 8. [27] |
Несмотря на очевидные различия в прочности кратной связи по сравнению с С-С - связью нафтенового кольца, обращают на себя внимание практически равные величины стабильности к электронному удару ( WM 18 1 - 18 7 %) для молекулы индана и изомерных ему алкенилбензолов. Причина такого сходства кроется, вероятно, в циклизации алкенильной цепи с кратной р-связью в пя-тичленное кольцо, завершающейся образованием устойчивой молекулы индена. [28]
Бензольное ядро реагирует с озоном значительно медленнее, чем этиленовая связь. Это позволяет окислять боковые цепи алкенилбензолов, не затрагивая ароматической части молекулы ( см., например, получение ванилина из изоэвгенола; стр. [29]
С получили нафталин, бензол, толуол, ксилолы и, возможно, этилбензол. Были также получены высшие алкилбензолы, алкенилбензолы в продуктах реакции отсутствовали. [30]
Страницы: 1 2 3