Алкиларилкетон
Cтраница 2
При нагревании алкиларилкетонов в запаянных ампулах с водными растворами полисульфида аммония или, проще, с серой и первичными или вторичными аминами ( чаще всего с морфолином) образуются амиды ( о-арилкарбоновых кислот или сами кислоты. [16]
Обратите внимание на то, что первый является смешанным алкиларилкетоном, второй - чисто ароматический кетон. [17]
Для бензофенонов характерны те же типы разрывов связей, что и для алкиларилкетонов. [18]
Следует отметить работу Майера и Мюллера, которые изучили замыкание кольца у алкиларилкетонов. Они нашли, что циклизация под действием концентрированной серной кислоты идет легко с образованием инданонов. [19]
Реакция ArCOOLi с RLi - это одна из стадий превращения ароматического альдегида в алкиларилкетон. [20]
Этот синтез, которому посвящен обзор [28], представляет собой общую реакцию для диарилкетонов, гексаалкилацетонов и mpem - алкиларилкетонов. Кетон расщепляется при кипячении с амидом натрия в углеводородных растворителях, например бензоле, толуоле или ксилоле. [21]
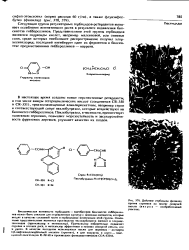 |
Действие гербицида фюзилад против сорняков на посеве сахарной свеклы ( вверху - необработанный участок. [22] |
В настоящее время созданы новые перспективные ретарданты, в том числе амиды гетероциклических кислот ( соединения CR-350 и CR-351), триазолзамещенные алкиларилкетоны, например строи и соответствующий спнрт паклобутразол, которые воздействуют на биосинтез гиббереллинов. Паклобутразол, в частности, препятствует полеганию зерновых, повышает морозостойкость и засухоустойчивость фруктовых деревьев, улучшает качество их плодов. [23]
Алкильные группы можно ввести в ароматическое ядро следующими способами: реакцией Вюрца-Фиттига или Зайцева-Гриньяра; аци-лированием ароматических углеводородов с последующим восстановлением образующихся алкиларилкетонов; алкилированием ароматических углеводородов галоидными алкилами, спиртами, простыми и сложными эфирами, парафинами или олефинами в присутствии катализаторов H2S04, H3P04, HF, ZnCl2, А1С13, FeCl3 BF3 и др. Из всех этих способов наибольший интерес, несомненно, представляет реакция алкилирования ароматических углеводородов олефинами. Эта реакция обеспечена дешевым и доступным сырьем, осуществляется по сравнительно простой технологической схеме и позволяет получить целевые продукты - алкил-ароматические углеводороды с хорошими выходами. Все это ставит ее вне конкуренции со всеми другими указанными выше способами и обеспечивает ей прекрасные перспективы дальнейшего развития. [24]
Шеглером и Адкинсом 417В описан удобный метод для получения первичных аминов, заключающийся в том, что альдегиды, ди-алкил - и алкиларилкетоны нагреваются при 125 - 150 со смесью из жидкого аммиака, метанола и водорода при 150 ат давления в присутствии катализатора Ренея. [25]
К такому типу превращений склонны, в частности, ароматические альдегиды, содержащие в ароматическом кольце электронодонорные группы, а также многие диарил - и алкиларилкетоны. [26]
Алкильные группы можно ввести в ароматическое ядро следующими способами: реакцией Вюрца - Фиттига или Зайцева - Гриньяра; ацилированием ароматических углеводородов с последующим восстановлением образующихся алкиларилкетонов: алки-лированием ароматических углеводородов галоидными алкиламта, спиртами, простыми и сложными эфирами, парафинами или олефинами в присутствии катализаторов H SO, , НзР04, HF, ZnCl-2, А1С1з, FeCl3, BF3 и др. Из всех этих способов наибольший интерес, несомненно, представляет реакция алкилирования ароматических углеводородов олефинами. Эта реакция обеспечена дешевым и доступным сырьем, осуществляется по сравнительно простой технологической схеме и позволяет получить целевые продукты - алиил-ароматические углеводороды с хорошими выходами. Есо это ставит ее вне конкуренции со всеми другими указанными выше способами и обеспечивает ей прекрасные перспективы дальнейшего развития. [27]
Этого типа реакция характерна-как для алифатических, так и для ароматических альдегидов и кетонов. Относительно восстановления алкиларилкетонов сведения почти отсутствуют. [28]
Этого типа реакция характерна как для алифатических, так и для ароматических альдегидов и кетонов. Относительно восстановления алкиларилкетонов сведения почти отсутствуют. [29]
Как правило, наиболее удобными являются оксимы, в которых один изомер более устойчив, чем другой, и взаимопревращение син - и ангы-изомеров затруднено. Этим требованиям отвечают оксимы алкиларилкетонов, в которых объемистая арильная группа занимает амги-положение и, следовательно, предпочтительнее к миграции, чем алкильная группа. Это обобщение имеет противоположный смысл, когда алкильная группа является более объемистой ( например, разветвленной), чем арильная, и, следовательно, алкильная группа становится в амги-положение. Оксимы диалкилкетонов обычно дают смесь амидов, так как взаимные переходы син - и анты-изомеров происходят относительно легко. Оксимы циклических кетонов также подвергаются перегруппировке Бек-мана, что является общепринятым методом синтеза макроцикличе-ских лактамов ( см. разд. [30]
Страницы: 1 2 3