Арила
Cтраница 2
В синтезе арил - и также алкилалкоксисиланов наиболее широко, как уже было показано, используются зтоксисиланы. Принципиально во-м ( Жно использование в этой реакции любого алкокси -, а также и ароксисилана. [16]
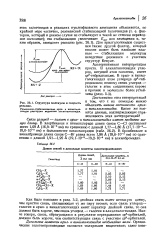 |
Структура молекулы и скорость. [17] |
Дипольные моменты арил - и винилгалогенидов необычайно малы. [18]
Под радикалом арил подразумевается С6Н5, / 7 - СН3С6Н4 р - С1С6Н4, / 7 - СН3ОСвН ( с соответствующими температурами распада, 200 в вакууме, 171 ( темп, пл. Соединения, образованные из циклопентадиена, ведут себя подобным же образом. Соединение, образованное циклопентеном, при нагревании только постепенно разлагается89 на составные ча ти. [19]
Фунгицидная активность арил - и алкиларсинов и их производных уменьшается с увеличением молекулярной массы соединения. [20]
Определению меди арил - и диарилтиосемикарбазидами мешают ионы двухвалентного олова, ионы перманганата, хромата и бихромата. [21]
Хлорал кил арил амины менее реакционноспособны, чем бромал-килариламины. Так, за 3 - 5 ч кипячения их выделено 52 - 68 % продукта, в то время как реакция с бромпроизводными идет даже при комнатной температуре ( 24 ч) и дает почти количественный выход. Реакция с иодпроизводными осложняется образованием побочных продуктов. С удлинением алкильной цепи реакционная способность галоидалкилариламинов несколько увеличивается. [22]
Приведены способы получения арил - и диарилтиосемикарбазидов. [23]
Таблицы по синтезу арил ( гетерил) нитроалкенов см. В. В. Перекалин, Непредельные нитросоединения. [24]
Другой метод синтеза арил ( Р р-диметоксиэтил) сульфидовт описанный Нандья и Тилаком [56, 60], заключается во взаимодействии ариллитиевых производных ( фениллития, 2-тиениллития, а-нафтиллития, 2-бензо [6] тиениллития, тиенил-2 5-дилития и др.) с р р р р - тетраметоксидиэтилдисульфидом. Последующая циклизация образующихся сульфидов в присутствии полифосфорной кислоты приводит с выходом 2 - 35 % к соответствующим конденсированным тиофенам и тиопиранам. [25]
Алкил ( реже арил) тиираны под действием гидридов металлов 1л, 51, 8п или орг. [26]
Предлагаемый метод синтеза арил - - нитровинилкетонов, по-видимому, является первым случаем получения нитросоединений алкилированием нитрит-аниона четвертичными аммониевыми солями. Несмотря на предпринимавшиеся попытки, нам не удалось получить арил - 3-нитровинилкетоны с о-заместителями, а также адкил - 3-нитровинилкетоны. [27]
Основные направления распада арил ( гетерил) кетонов в ряду гетероароматических соединений подобны фрагментации диа-рилкетонов и связаны с а-разрывами. При этом заряд в зависимости от стабильности образующегося иона преимущественно локализуется на фрагменте, содержащем арильную группу либо гетероцикл. [28]
Основным направлением распада арил ( циклоалкил) сульфидов является выброс из М - молекулы циклоалкена в результате процесса, подобного перегруппировке Мак-Лафферти. [29]
В ИК спектрах арил - и алкилазидов проявляются асим-метрич. [30]
Страницы: 1 2 3 4