Комплекс - кислота
Cтраница 2
Дрью и Файрбайрн выделили два главных типа комплексов азо-салициловых кислот; один из них, в котором два атома хрома связаны с тремя молекулами азосалициловой кислоты ( III), принадлежит к тому же типу, что и комплекс ( I), полученный ранее Морганом и Майн Смитом. [16]
Сопоставление устойчивости комплексов этилендиаминди-изопропилкарбоновой кислоты с устойчивостью аналогично построенных комплексов этилендиаминдиметилкарбоновой кислоты показывает, что комплексы этилендиаминдиизопро-пилкарбоновой кислоты менее устойчивы. [17]
Шварценбах, Сенн и Андерег [30] нашли, что у комплексов полиметилендиаминтетрауксусных кислот с двухвалентной ртутью значения констант устойчивости сперва падают, а потом возрастают по мере увеличения числа полиметиленовых членов. С ростом числа членов, правда, уменьшается вероятность образования циклов, но увеличивается его прочность, так как оба атома азота могут занимать противоположные места. [18]
В монографии К. П. Ядимирского с сотрудниками [180] обобщен материал по изучению комплексов о-фенолкарбоно-вых кислот с редкоземельными элементами. Данные этих авторов, а также рассмотренный в обзоре материал свидетельствует о том, что строение комплексов о-фенолкарбоновых кислот трифенилметанового ряда находится лишь в начальной стадии изучения. Для решения данного вопроса необходимо привлечение различных физических методов исследования. [19]
Это заставляет допустить, что предполагаемый промежуточный продукт реакции ( 1) - комплекс щаве-левоянтарной кислоты с ферментом - не способен легко диссоциировать. Между лимонной кислотой и НАДФ осуществляется непосредственный перенос водорода, который стереоспецифичен по отношению к Л - стороне никотинамидного кольца НАДФ ( см. стр. Сторону никотинамидного кольца определяют по сте-реоизомеру НАДФ-D, который после гидролитического отщепления фосфата дает НАД-D с дейтерием на Л - стороне кольца. [20]
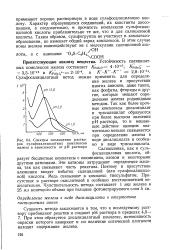 |
Спектры поглощения раство - виде дисалицилата и особен-ров сульфосалицилатных комплексов но в ввде трисалицилата. железа в зависимости от рН раствора Салициловая, как И суль. [21] |
Характер образующихся соединений, их константы диссоциации, а следовательно, и прочность комплексов сульфосали-циловой кислоты приблизительно те же, что и для салициловой кислоты. Таким образом, сульфогруппа не участвует в комплексо-образовании, но изменяет общий заряд комплексов. [22]
Сопоставление устойчивости комплексов этилендиаминди-изопропилкарбоновой кислоты с устойчивостью аналогично построенных комплексов этилендиаминдиметилкарбоновой кислоты показывает, что комплексы этилендиаминдиизопро-пилкарбоновой кислоты менее устойчивы. [23]
Согласно Пирсону [541-543] многие неорганические и органические соединения в твердом, жидком и газообразном состоянии представляют собой комплексы льюисовых кислот и оснований. Например, MgQ2 в твердом состоянии состоит из кислоты Mg2 координированной шестью соседними С1 - - ионами - лигандами, проявляющими свойства основания. [24]
В Институте нефти АН СССР была спроектирована н построена опытная установка для исследования реакции алкилирования бензола оле-фииами с помощью комплекса ортофосфориой кислоты и фтористого бора. Эксперименты па установке проводились при 50; было выяснено влияние молярного отношения бензол: непредельные н скорости подачи газа. [25]
Близкое расположение максимумов поглощения на спектрах разных кислот не позволяет путем непосредственного измерения поглощения в этих точках получить точные данные для всего комплекса кислот с сопряженными двойными связями или для каждой кислоты в отдельности. Однако все кислоты канифоли с сопряженными двойными связями изомеризуются после обработки минеральной кислотой, образуя абиетиновую кислоту или равновесную смесь, содержащую в основном абиетиновую кислоту. [26]
Важное значение для развития представлений о механизме кто-лотно-основных взаимодействий, каталитических процессов в жидкой фазе и на поверхности твердого тела имеет исследование комплексов кислот с водой и другими кислородсодержащими молекулами. В системах галоидоводороды - диме-тиловый эфир в азотной матрице зарегистрированы ИК-спектры молекулярных комплексов НС1 и НВг с эфиром, которые находятся в равновесии с ионными комплексами типа [ МеаОНОМег. В работе [55] отмечается, что комплексы HClOi, и НМ03 с CHjNOg и ( CH3) 2NCHO имеют молекулярную структуру, но комплекс HN03 с ( CH3) eSO при - 180 С - ионный. При нагревании происходит обратный переход протона к нитрат-иону. [27]
Спектроскопически было показано, что сопряжение в ароматическом амине при образовании комплексов с этими кислотами нарушается и дипольные моменты межмолекулярных связей в комплексах кислот с алифатическими и ароматическими аминами близки между собой. Разность между теплотами образования комплексов кислоты с алифатическим и ароматическим аминами характеризует энергию ря-сопряжения в молекуле амина. Найденные значения оказались близки к значениям, приведенным для диметилани-лина в табл. V.10, которые были получены при исследовании ком-плексообразования с галогенидами элементов III группы. [28]
При замене водорода в иминодиуксусной кислоте ( ИДА) на группу - СН3 основность атома азота повышается, что проявляется в увеличении pk2, а следовательно, и прочности комплексов метил-иминодиуксусной кислоты по сравнению с комплексами пминодиук-сусной кислоты. [29]
При замене водорода в иминодиуксусной кислоте ( ИДА) на группу - СН3 основность атома азота повышается, что проявляется в увеличении pk2, а следовательно, и прочности комплексов метил-иминодиуксусной кислоты по сравнению с комплексами пминодиук-сусной кислоты. [30]
Страницы: 1 2 3 4