Комплекс - бор
Cтраница 2
Все же было бы преждевременно на основании этих данных утвер - ждать, что комплексы бора и бериллия всегда характеризуются наличием именно тетраэдрической конфигурации. [16]
Измерение интенсивности люминесценции нужно производить в первый момент облучения растворов светом, так как в дальнейшем под его действием интенсивность люминесценции комплекса бора с бензоином постепенно снижается. В связи с этим до момента измерения кюветы следует закрывать сверху пластинками из материала, не пропускающего возбуждающего света. [17]
Метод основан на отделении бора от олова и содержащихся в нем микропримесей тяжелых металлов и флуоресцентном его определении по интенсивности свечения комплекса бора с бензоином в этанольном растворе. [18]
Измерение интенсивности флуоресценции нужно проводить в первый момент облучения растворов ультрафиолетовым светом, так как в дальнейшем под действием ультрафиолетовых лучей интенсивность флуоресценции комплекса бора с бензоином постепенно снижается. В связи с этим до момента измерения кюветы следует закрывать сверху пластинками из материала, не пропускающего ультрафиолетовых лучей. [19]
Измерение интенсивности флуоресценции нужно проводить в первый момент облучения растворов ультрафиолетовым светом, так как в дальнейшем под действием ультрафиолетовых лучей интенсивность флуоресценции комплекса бора с бензоином постепенно снижается. В связи с этим до момента измерения кюветы следует закрывать сверху пластинками из материала, не пропускающего ультрафиолетовых лучей. [20]
Однако для пломбировочных материалов наиболее интересны методы отверждения эпоксидных смол под действием инициаторов катионной полимеризации, к которым следует отнести наиболее широко применяющиеся кислоты Льюиса и их комплексы с различными соединениями, главным образом, комплексы трехфтори-стого бора. [21]
Образец, содержащий не менее 1 мг / см3 бора, сплавляют при 800 С с карбонатом натрия и пероксидом натрия. Концентрацию комплекса бора с маннитом определяют по разности объемов титранта, соответствующих двум конечным точкам титрования, с учетом поправки на фон, вносимый маннитом. [22]
Вследствие собственной окраски реагентов в обоих методах наблюдается сильное поглощение растворов сравнения. Окраска комплекса бора с этими реагентами разрушается прежде всего под действием окислителей ( а также нитрата) фтора. Хотя другие катионы мешают незначительно, во многих случаях проводят предварительное отделение борной кислоты дистилляцией. [23]
При той высокой кислотности ( почти концентрированная H2S04), при которой выполняются цветные реакции на бор с ( поли) оксиантрахинонами, бор присутствует в растворах в виде солей катиона борила, а оксиантрахиноны - частично в виде оксониевых солей. Такие же ионные состояния существуют и в комплексах бора с оксиантрахинонами, где, кроме того, имеется частично ионная связь между бором и фенольным кислородом. [24]
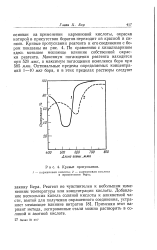 |
Кривые пропускания. [25] |
По сравнению с хинализарином здесь меньшее мешающе влияние собственной окраски реагента. Максимум поглощения реагента находится при 520 ммк, а максимум поглощения комплекса бора при 585 ммк. [26]
В самом деле, химические сдвиги ИВ во всех соединениях бора, изученных до настоящего времени с помощью метода ядерного магнитного резонанса на ПВ, лежат между этими двумя величинами. Исключения известны только для атома бора в вершине в пентаборане ВвНэ и для некоторых комплексов трехиодистого бора [5]; в этих соединениях резонанс на И. В имеет место даже в более сильном поле, чем в боргидридном ионе. Влияние растворителей на химические сдвиги ПВ в спектре ядерного магнитного резонанса, по-видимому, ничтожно мало, кроме случая, когда между соединением, содержащим бор, и растворителем протекает реакция. [27]
В самом деле, химические сдвиги ИВ во всех соединениях бора, изученных до настоящего времени с помощью метода ядерного магнитного резонанса на ИВ, лежат между этими двумя величинами. Исключения известны только для атома бора в вершине в пентаборане BsHg и для некоторых комплексов трехиодистого бора [5]; в этих соединениях резонанс на ПВ имеет место даже в более сильном поле, чем в боргидридном ионе. Влияние растворителей на химические сдвиги В в спектре ядерного магнитного резонанса, по-видимому, ничтожно мало, кроме случая, когда между соединением, содержащим бор, и растворителем протекает реакция. [28]
При флуориметрировании веществ, совершенно прозрачных для видимого света, возбуждение лампой накаливания сравнительно менее эффективно. Однако и в этом случае то относительно небольшое количество ультрафиолетовых излучений, которое находится в непрерывном спектре лампы накаливания, оказывается достаточным для количественного флуоресцентного определения с удовлетворительной чувствительностью таких веществ, как хинин, комплекс бора с бензоином, некоторые витамины, растворы битумов в хлороформе и им подобные. Для возбуждения веществ, имеющих спектры поглощения в более далекой ультрафиолетовой области, следует применять ртутно-кварцевые лампы со светофильтрами, выделяющими излучения, по возможности близкие к максимуму поглощения анализируемого вещества. Для работы в еще более коротковолновой области целесообразно использовать газоразрядные водородные или аргоново-криптоновые лампы со сплошным спектром испускания. [29]
В первых двух методах измерения проводят в среде 95 % - ной H2SO4 при 615 нм и в смеси H2SO4 - уксусная кислота при 548 нм. Чувствительность определения равна соответственно 1 5 - 10 - 3 и 3 8 - 10 - 4 мкг / мл. На рис. 7 приведены спектры поглощения комплексов бора с карминовой кислотой, из которых видно, что поглощение в УФ-области ( 300 нм) выше, чем в области 600 - 615 нм. Чувствительность определения В при 300 нм равна 7 - 10 - 4 мкг / мл. [30]
Страницы: 1 2 3