Белковый комплекс
Cтраница 1
 |
Реконструкция частиц ВТМ из субъединиц белка оболочки и молекулы вирусной РНК. [1] |
Крупные надмолекулярные белковые комплексы являются самоорганизующимися системами. Характерный примертакого рода - система синтетаз жирных кислот ( из дрожжей), состоящая из 7 различных ферментов. Каждый из этих ферментов, в свою очередь, построен из 3 - х, по-видимому, идентичных субъединиц. [2]
Актомиозин - белковый комплекс, который образуется при смешивании актина и миозина. В присутствии АТФ и Mg актомиозиновый комплекс диссоциирует с резким снижением вязкости. [3]
Цитохромоксидаза представляет собой сложный белковый комплекс, в состав которого входит по меньшей мере 8 индивидуальных полипептидов. Во внутримолекулярном переносе электронов участвуют простетические группы фермента: темы я и аз, а также 2 атома меди: Сид и Сив - Трансмембранный перенос электронов от цитохрома с к молекулярному кислороду сопровождается векторным переносом протона из матрикса митохондрий в межмембранное пространство. Разность электрохимических потенциалов ионов водорода, генерируемая в цитохромоксидазной реакции на мембране митохондрий, может быть использована для синтеза АТФ. [4]
После диссоциации белкового комплекса гранс-ретиналь восстанавливается до соответствующего ретинола, который ферментными системами вновь превращается в 11-чмс-ретиналь. Потери витамина А, происходящие в этом процессе, восполняются из печени. [5]
Уменьшение внешней поверхности белковых комплексов под влиянием денатурации приводит к сокращению связей взаимодействующих с молекулами глицеридов. По этой причине масло на денатурированной поверхности белка располагается в виде полимолекулярных слоев. [6]
В высших организмах присутствует белковый комплекс, осуществляющий специфич. АТФ в обмен на АДФ ( транслоказа адениновых нуклеоти-дов) и являющийся первым хорошо изученным белком-переносчиком. Особая роль аденозин-5 - фосфорных к-т в биоэнергетике обусловливает то, что эти соед. [7]
Необратимая димеризацпя н образование белковых комплексов объясняется чисто химическими реакциями. Так, серумальбумин содержит SH-группу, легко реагирующую с ионом ртути. В присутствии ртутных солей происходит димери-зация альбумина через атом ртути по принципу А-S - Hg-S - А. Получается как бы новый белок двойного молекулярного веса - меркаптальбумин. Иногда изменение четвертичной структуры сильно сказывается на функциональной активности белка. Так, например, фермент дегидрогеназа фосфоглицеринового альдегида ( из мышц кролика) содержит SH-грушгу. При окислении воздухом белок димеризуется через дисульфидный мостик, утрачивая активность. При восстановлении дисульфидного мостика п-роисходит полное восстановление активности. С другой стороны, простое устранение сульфгидрильной группы без димеризации не ликвидирует ферментативную активность. [8]
Фактор сопряжения F, представляет собой белковый комплекс, содержащий девять субъединиц: три одинаковых а субъединиц, три одинаковых / 3 субъединиц и по одной j, 6 и е субъединиц. Фактор F, имеет вращательную симметрию третьего порядка. Поворот вокруг оси, параллельной 7 субъединице, приводит к смещению каждой из а и / 3 субъединиц в положение другой аналогичной субъединицы. Небольшая субъединица е является регулятором ферментативной активности. [9]
Во время хранения продуктов в белковом комплексе под влиянием гидролитических ферментов, которые содержатся в самом продукте, происходит автолитический распад белка; в результате образуются аминокислоты, а иногда и более простые продукты со щелочными свойствами. Простейшая схема разложения белков: протеины - альбумозы и пептоны - полипептиды - аминокислоты. [10]
Рассмотрим, каким образом в природе несимметричный мак-лярный белковый комплекс участвует в синтезе этого циклического полипептида без помощи рибосом. Механизм синтеза, присущий лишь простым организмам, подобным бактериям, расшифрован биохимиком Липманом. [11]
Предполагается, что расплетающий эффект кэпсвязывающего белкового комплекса зависит от АТФ, и что гидролиз АТФ требуется для такого расплетания. [12]
Витамин Bia, связанный в таком белковом комплексе, становится недоступным для микробов желудочно-кишечного тракта, которые потребляют этот витамин. У больных злокачественной анемией в желудочном соке белок, необходимый для образования комплекса с витамином Ви, отсутствует. В этом случае использование витамина Bi2 микробами уменьшает количество витамина, поступающего в ткани животного организма, и таким путем способствует возникновению авитаминоза. Однако возможно, что указанный белок как-то облегчает всасывание кобаламина в кишечнике. Эти данные представили новое объяснение связи, которая существует между развитием злокачественной анемии и нарушением функции желудка. [13]
Сам трехвалентный хром, хотя и образует белковые комплексы, но они не обладают антигенной активностью или обладают ею в слабой степени. [14]
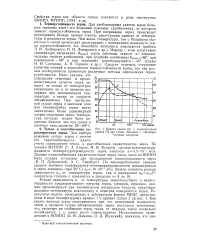 |
Кривая сушки ( 2 и температурная кривая ( 1 при сушке пшеницы с предварительным нагревом. [15] |
Страницы: 1 2 3 4