Отрицательно заряженный комплекс
Cтраница 3
При этом никель, хром, алюминий и другие элементы, не образующие отрицательно заряженных комплексов, уходят в фильтрат, а железо и медь сорбируются анионитом. При этом железо и медь проходят в фильтрат. [31]
Никель, хром, марганец, алюминий как не образующие в этих условиях отрицательно заряженных комплексов переходят в фильтрат, а железо и медь сорбируются анионитом. [32]
Образовавшийся положительно заряженный водород или снова взаимодействует с олефином, или присоединяется к отрицательно заряженному комплексу ( О8ОзН) -, образуя серную кислоту. Таким образом, либо реакция будет продолжаться дальше, либо восстанавливается исходная серная кислота. В идеальном случае в процессе полимеризации, как это видно и из приведенного примера, серная кислота как катализатор не должна подвергаться каким-либо изменениям. [33]
После расщепления связи бром - бром образуется а-комп-лекс с бензолом, от которого возникающий отрицательно заряженный комплекс - Вг - РеВг3 отрывает протон, давая бром-бензол. [34]
В тех случаях, когда необходимо разделить нейтральные моносахариды, используют их способность образовывать отрицательно заряженные комплексы с борной кислотой или ее солями33 65, с молибдатами36, вольфраматами, германа-тами 37 и рядом других неорганических анионов; разные анионы предъявляют часто различные требования к стереохимии моносахарида, необходимой для образования устойчивых комплексов. Для обнаружения зон веществ на электрофореграм-мах применяется большинство реагентов, используемых при хроматографии на бумаге. [35]
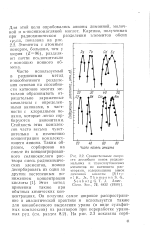
Часто используемый в радиохимии метод ионообменного разделения основан на способности катионов многих металлов образовывать отрицательно заряженные комплексы с определенными анионами, в частности с хлоридными ионами, которые легко сорбируются анионитами. Стойкость этих комплексов часто весьма чувствительна к изменению концентрации комплексующего аниона. Этот метод применим также при обычных химических концентрациях. [37]
Для десорбции применяют концентрированные растворы соляной и азотной кислот, в которых плутоний образует отрицательно заряженные комплексы. [38]
После расщепления связи бром - бром образуется а-комп-лекс с бензолом, от которого возникающий отрицательно заряженный комплекс Вг-РеВгз отрывает протон, давая бром-бензол. [39]
Никель, хром, ванадий, молибден, алюминий, железо как не образующие отрицательно заряженных комплексов, переходят в фильтрат, а цинк и свинец сорбируются анионитом. Вольфрам или ниобий, если они присутствуют в сплаве, предварительно отделяют кислым гидролизом или переводят в комплексные соединения. [40]
При этом кобальт, железо и другие элементы сорбируются, а никель, не образующий отрицательно заряженных комплексов, переходит в фильтрат. В фильтрате, никель определяют фотоколориметрическим методом в виде диметилглиоксимата никеля. [41]
Уменьшение сорбируемости меди с дальнейшим ростом концентрации адденда связано с образованием в растворе незаряженных и отрицательно заряженных комплексов. [42]
Авторы высказывают предположение, что низкая скорость катодного процесса в безводном диметилацетамиде связана с существованием отрицательно заряженных комплексов цинка, которые практически не разряжаются либо из-за их прочности, либо из-за электростатического отталкивания от одноименно заряженной поверхности электрода. Второе предположение наиболее вероятно, так как при введении воды в растворитель молекулы ее, обладая более высоким дипольным моментом ( енго81; едмА36 7), снижают заряд комплекса, вытесняя хлорид-ионы из внутренней сферы и образуют электрохимически активные частицы. [43]
Авторы высказывают предположение, что низкая скорость катодного процесса в безводном диметилацетамиде связана с существованием отрицательно заряженных комплексов цинка, которые практически не разряжаются либо из-за их прочности, либо из-за электростатического отталкивания от одноименно заряженной поверхности электрода. Второе предположение наиболее вероятно, так как при введении воды в растворитель молекулы ее, обладая более высоким дипольным моментом ( ен о - 81; едмд - 36 7), снижают заряд комплекса, вытесняя хлорид-ионы из внутренней сферы и образуют электрохимически активные частицы. [44]
Таким образом, выводы о строении ионных пар, образуемых неорганическими и органическими катионами с отрицательно заряженными комплексами Со ( С2О4) д и 1гС1д -, хорошо согласуются. Соответственно, приведенные в работе [160] и табл. III.5 сведения о константах устойчивости ионных пар, образуемых сферически симметричными комплексами IrClj - и Со ( СаО4) з - с различными катионами, могут быть использованы для оценки степени ассоциации других похожих комплексных анионов с катионами. [45]
Страницы: 1 2 3 4