Красный комплекс
Cтраница 1
Красный комплекс содержит две пероксидные группы. [1]
Красный комплекс железо ( III) - аммонийный роданид, образующийся в результате реакции между органической перекисью и роданидом железа ( II), был использован для количественного анализа. В одной из методик230 предложено визуально сравнивать его окраску со стандартными растворами, содержащими перманганат и бихромат калия. [2]
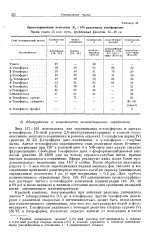 |
Ориентировочные величины Rf X 100 различных токоферолов. [3] |
Красный комплекс, получающийся при действии реактива дипиридила железа ( обнаруживается 0 5 is а-токоферола; другие токоферолы реагируют с различной скоростью и интенсивностью), может быть использован для количественного определения, для чего его экстрагируют водой и фото-метрируют. [4]
Красный комплекс, получающийся при действии реактива дипиридила железа ( обнаруживается 0 5 и г а-токоферола; другие токоферолы реагируют с различной скоростью и интенсивностью), может быть использован для количественного опрзделения, для чего его экстрагируют водой и фото-метрируют. [5]
Красный комплекс никеля ( II) мало растворим, красный комплекс Fe2 хорошо растворим. Окраска комплекса исчезает при окислении Fe ( II) в Fe ( III) перекисью водорода. [6]
Красные комплексы цинка и кадмия с ПАН экстрагируют хлороформом. Экстракт обрабатывают диэтилдитиокарбаминатом натрия; при этом комплекс цинка остается без изменений, тогда как комплекс кадмия разрушается с образованием дитиокарбаминатно-го комплекса желтого цвета. На этом основан метод определения цинка и кадмия при их совместном присутствии. Максимум светопоглощения комплекса индия с ПАН в хлороформе находится при 530 и 560 ммк, аналогичный комплекс железа ( III) имеет максимум при 525 и 775 ммк. Комплекс индия при 775 ммк совсем не поглощает, что позволяет одновременно определять индий и железо. [7]
Красный комплекс железа ( II) с 1 10-фенантролином образует окрашенные экстрагируемые соли с анионами некоторых органических кислот. В качестве примера приводится способ определения трихлоруксусной кислоты. Полученный раствор взбалтывают 5 мин с 10 мл нитробензола. Отстоявшийся органический слой, содержащий [ Fe ( phen) 3 ] ( СС13СОО) 2, взбалтывают до просветления с 1г безводного Na2SO4 и измеряют оптическую плотность при 516 нм. [8]
Красные комплексы металлов с мурексидом менее устойчивы, чем комплексы этих металлов с ЭДТА. [9]
Красный комплекс палладия с реагентом образуется мгновенно. Он нерастворим в воде, и поэтому необходимо добавление ацетона или метилцеллозольва. Этот метод считают ошибочно более чувствительным, чем метод с использованием л-нитрозодифенилами-на. Последний характеризуется более низким открываемым минимумом. Избирательность и область применимости висмутиола II примерно такие же, как и у других уже упомянутых меркаптанов. Ни один из этих реагентов не имеет преимуществ по сравнению с общепринятыми реагентами. [10]
Красные комплексы металлов с мурексидом менее устойчивы, чем комплексы этих металлов с ЭДТА. [11]
Стабильный красный комплекс состава 2: 1 с максимумом светопоглощения 548 нм образуется в разбавленном растворе соли кальция. В присутствии больших количеств кальция возникает значительно менее стабильный фиолетовый комплекс состава 1: 1 с максимумом светопоглощения 750 нм. [12]
Образовавшийся красный комплекс кобальта хорошо экстрагируется хлороформом, четыреххлористым углеродом, бензолом, толуолом, кем лолом, амилацетатом и другими растворителями. [13]
Образующийся красный комплекс меди устойчив только в отсутствие свободных ионов водорода и сильных комплексообразователей. [14]
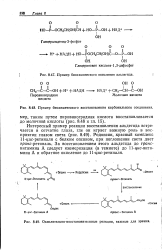 |
Пример биохимического восстановления карбонильного соединения.| Окислительно-восстановительные реакции, важные для зрения. [15] |
Страницы: 1 2 3 4