Красный комплекс
Cтраница 2
Родопсин, красный комплекс 11 - Ч с-ретиналя с белком опсином, при поглощении света дает гранс-ретиналь. За восстановлением этого альдегида до транс-витамина А следует изомеризация ( в темноте) до 11 - мс-вита-мина А и обратное окисление до 11 - г ыс-ретиналя. [16]
Максимум поглощения красного комплекса родия с хлоридом олова находится при 470 нм. [17]
В образующемся красном комплексе - хелате - имеется координационная связь иона металла с атомом азота азогруппы и валентная с двумя оксигруппами в о-положении к ней. Устойчивость комплексов металлов с металлоинди-катором должна быть меньше устойчивости соответствующих комплексонатов. На рис. 15.8 в качестве примера приведены электронные спектры поглощения эриохромового черного Т и его комплекса с магнием. Из них следует, что свободный индикатор наиболее интенсивно поглощает лучи красного цвета и имеет, следовательно, синюю окраску. Комплекс магния с реагентом более погло: щает желто-зеленое излучение и поэтому отличается красно-фиолетовой окраской. [18]
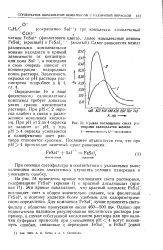 |
Кривая поглощения света растворами салицилатов железа. [19] |
Эти кривые показывают, что красный комплекс FeSal поглощает свет в общем значительно сильнее, чем фиолетовый FeSal, и поэтому является более удобным для колориметрического определения. [20]
Роданид образует с ионами Fe111 интенсивно окрашенные красные комплексы. [21]
ДП дает с Fe2 водорастворимый глубоко окрашенный красный комплекс. [22]
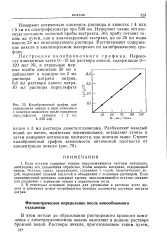 |
Калибровочный график для определения никеля в виде комплекса с диметилглиоксимом после окисления персульфатом ( кюветы / 2 Я 530 нм. [23] |
В этом методе до образования растворимого красного комплекса с диметилглиоксимом никель окисляют в водном растворе бромной водой. [24]
Для фотометрического определения титана чаще используют красный комплекс, как более прочный; оптическую плотность измеряют при 520 ммк, где больше разница свето-поглощений красного и желтого комплексов. [25]
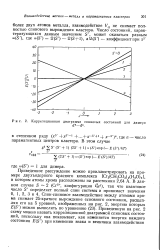 |
Корреляционная диаграмма спиновых состояний для димера. [26] |
Приведенное рассуждение можно проиллюстрировать на примере двухъядерного красного комплекса [ Сг2 ( СН3СО2) 4 ( 1 0) 2 ], в котором атомы хрома расположены на расстоянии 2 64 А. [27]
Метод основан на колориметрическом определении интенсивности окраски красного комплекса железа с о-фенантролином. [28]
Красный комплекс никеля ( II) мало растворим, красный комплекс Fe2 хорошо растворим. Окраска комплекса исчезает при окислении Fe ( II) в Fe ( III) перекисью водорода. [29]
Некоторые нитросоединения при обработке гидроксидом натрия образуют оранжевые или красные комплексы ( разд. Амиды и имиды при действии гидроксида натрия могут отщеплять аммиак или амины ( разд. Эти реакции, по существу, позволяют определить тип функциональных групп, которые могут содержать азот. Поэтому присутствие этих групп следует ожидать при положительных реакциях на азот. [30]
Страницы: 1 2 3 4