Красный комплекс
Cтраница 3
Соединения этого типа получены и для других галоидов: красный комплекс [ TcR2Br2 ] Br и темно-красный - [ TcR2I2 ] I-12. В этих комплексах валентное состояние технеция более устойчиво, чем в соответствующих комплексах трехвалентного рения. Например, ион Се4 окисляет рений в подобных соединениях, в то время как технеций остается без изменения. [31]
Соединения этого типа получены и для других галоидов: красный комплекс [ TcR2Br2 ] Br и темно-красный - [ TcR2I2 ] I - I2 - В этих комплексах валентное состояние технеция более устойчиво, чем в соответствующих комплексах трехвалентного рения. Например, ион Се4 окисляет рений в подобных соединениях, в то время как технеций остается без изменения. [32]
После отгитровывания ионов Ag избыток титранта дает с ионами Fe3 красный комплекс. Титрование проводят в кислой среде. [33]
Проба с цериевым реактивом отрицательна [3], т.е. не образуется красный комплекс и сохраняется желтый цвет реактива в случае альдегидов, ке-тонов, предельных и непредельных кислот, сложных и простых эфиров, двух - и трехосновных карбоновых кислот. [34]
Если она существует в таком виде, тогда структурная формула красного комплекса может соответствовать написанной. [35]
Так, при титровании пробы воды трилоном Б в присутствии эриохрома черного красные комплексы кальция и магния разрушаются, образуются комплексонаты этих металлов с трилоном Б, не имеющие окраски. [36]
Мочевина образует с диацилмонооксимом в присутствии тиосемикарбазида и ионов Fe3 в сильнокислой среде красный комплекс, который фотометрируют. [37]
Стил и йо [587] применяли этот реактив, образующий растворимый в воде, устойчивый красный комплекс состава R2RuO4 с максимумом светопоглощения при 530 ммк, для определения 0 5 - 14 мкг / мл рутения. Окраска при комнатной температуре развивается мгновенно. Рекомендуемые кислотность и количество реагента можно не соблюдать слишком строго. Кислотность поглощающего раствора выбирают с таким расчетом, чтобы ион рутената не разложился. Определению мешают многие примеси, поэтому необходима отгонка рутения. Осмий также взаимодействует с этим реагентом, образуя комплексное соединение, пригодное для спектрофотометри-ческого определения. Поэтому растворы предварительно кипятят с азотной кислотой для удаления осмия. [38]
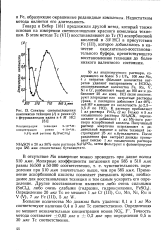 |
Спектры светопоглощения. [39] |
Говард и Вебер [181] предложили другой метод, который также основан на измерении светопоглощения красного комплекса технеция. [40]
Этот реактив представляет собой окрашенный в желтый цвет раствор аммонийгексанитратоцерата в разбавленной азотной кислоте и образует красные комплексы с соединениями, содержащими спиртовую гидроксильную группу. Положительную реакцию с этим реактивом дают первичные, вторичные и третичные спирты, содержащие до 10 атомов углерода. Кроме того, красное окрашивание характерно для всех типов гликолей, поли-олов, углеводов, оксикислот, оксиальдегидов и оксикетонов. [41]
При встряхивании синего раствора эрио OS в бутаноле с раствором соли индия при рН 10 образуется красный комплекс, переходящий в органическую фазу. По опытам Долежал, Шир и Яначек [166, 167] мурексид и эрио-хромцианин непригодны в качестве индикаторов для комплексонометрического титрования индия. Точку эквивалентности можно устанавливать амперометрически при помощи капельного ртутного катода. [42]
Наиболее важный из спектрофотометрических методов определения карбоксилсодержащих соединений основан на измерении сильного поглощения, характерного для красных комплексов железа и гидроксамовых кислот. [43]
Наиболее важный из фотометрических методов определения кислородсодержащих соединений основан на измерении сильного поглощения, характерного для красных комплексов железа и гидроксамовых кислот. [44]
Наиболее важный из спектрофотометрических методов определения карбоксилсодержащих соединений основан на измерении сильного поглощения, характерного для красных комплексов железа и гидроксамовых кислот. [45]
Страницы: 1 2 3 4