Диен
Cтраница 2
Простейший моноциклический диен циклобутадиен - нестабильное соединение и может участвовать в реакции Дильса - Альдера или в момент образования или при разрушении я-комп-лекса, в котором циклобутадиен стабилизуется. [16]
Исходным диеном по этому способу является бутадиен-1 3 ( дивинил), путем каталитической полимеризации которого получают полибутадиеновый каучук ( СКЬ); в свою очередь бутадиен-1 3 по методу Лебедева производят из этилового спирта. [17]
Исходным диеном по чтому способу является бута икч - 1 3 ( дивинил), путем каталитической полимеризации которого получают полпбутадпеповый каучук ( СКВ); в свою очередь бутадисн-1 3 по методу Лебедева производят из этилового спирта. [18]
Этот диен, по-видимому, образуется при переносе водорода с этилена на внутренний углеродный атом бутедиена по типу 1 2-присоединения. Факт существования а-алкил - или я-кротилже-леза не согласуется с образованием такого диена, не имеющего концевых метильных групп. [19]
Этот диен является весьма эффективным донором водорода, так как, теряя два атома водорода, он превращается в бензол, ароматическая система которого очень стабильна. Описанный метод не имеет преимуществ по сравнению с обычным гидрированием, за исключением-того, что для его проведения не нужна специальная аппаратура. [20]
Когда диен и диенофил являются полностью симметричными, как, например, при конденсациях бутадиена с этиленом или тетрацианэтиленом, возможно возникновение лишь одного переходного состояния, приводящего к одному аддукту. Но если хотя бы один из компонентов реакции не симметричен, становятся возможными несколько различных переходных состояний, приводящих к различным продуктам реакции. Разные виды асимметрии переходного состояния и обусловливают характерные особенности протекания диенового синтеза. [21]
Если диен или диенофил не симметричны относительно плоскости, проходящей через заместители участвующих в реакции двойных связей ( плоскости А и В), может проявиться третья особенность пространственной ориентации при диеновом синтезе - присоединение с наименее экранированной стороны. [22]
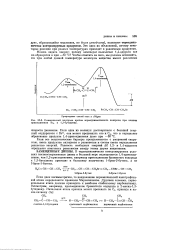 |
Кинетический контроль против термодинамического контроля при ионном присоединении Вг2 к 1 3 - 6утадиену. [23] |
Если диен несимметричен, то направление первоначальной электрофиль-ной атаки определяется правилом Марковникова. Другими словами, первоначальная атака должна приводить к наиболее стабильному карбокатиону. Рассмотрим, например, присоединение бромистого водорода к 2-метил - 1 3-бутадиену. [24]
Этот диен, по-видимому, образуется при переносе водорода с этилена на внутренний углеродный атом бутедиена по типу 1 2-присоединения. Факт существования о-алкил - или я-кротилже-леза не согласуется с образованием такого диена, не имеющего концевых метальных групп. [25]
Если диен в стадии координации участвует как бидентатный лиганд, то первичная реакция вхождения его в цепь приводит к образованию антизвена, которое изомеризуется в сын-звено. Если константа скорости роста ( fei) значительно выше константы скорости изомеризации ( &2), то формирующаяся цепь будет построена из цыс-звеньев. В тех случаях, когда скорость роста цепи находится в какой-либо зависимости от концентрации мономера, следует ожидать, что при малой концентрации мономера должно наблюдаться существенное повышение количества гранс-звеньев. [26]
Такой диен мог бы образоваться через 7 8-окись и полученное из нее 8-окси - 7-кетосоедине-ние. Значение максимума поглощения соответствует формуле XIII ( вычислено 249 тц); однако Бартон5 8 отметил аномальное значение разности молекулярных вращений полученного диена и холестана. Ненормально и то, что диен слабо вращает плоскость поляризации вправо, в то время как диеновые соединения с двойными: связями в положении-6 7 и 8 14 обычно сильно вращают влево. [27]
Как диен, так и триен можно получить в виде индивидуальных веществ. При нагревании чистых таутомерных форм до 100 образуется равновесная смесь валентных таутомеров, о которой шла речь выше. [28]
Если диен несимметричен, могут образоваться два продукта 1 2-присоединения. [29]
Если диен берется в двукратном количестве, то бициклопентеновое производное присоединяется к его следующей молекуле ( VI) Ц53 ( Ы ( ср. [30]
Страницы: 1 2 3 4