Промежуточная структура
Cтраница 2
В возникшей промежуточной структуре ( показанной в квадратных скобках, что символизирует переходный комплекс) валентность правого атома углерода полностью насыщена, а у левого атома углерода имеется только секстет электронов. Рассматриваемую переходную частицу, несущую положительный заряд, называют ионом карбония. Эта частица неустойчива и обладает большой реакционной способностью, так как ей необходим донор электронной пары, чтобы насытить ее валентные возможности. В рассматриваемом случае таким донором электронной пары оказывается хлорид-ион, образуемый реагентом НС1, и поэтому между ионом карбония и хлорид-ионом возникает химическая связь. [16]
Обладая промежуточной структурой между периленом и короненом 1 12-бензперилен по спектральным характеристикам существенно отличается от этих углеводородов. Интенсивная р-полоса ( lg е 4 - 4 5) расположена в области 3900 - 3300 А; а самая интенсивная Р - полоса начинается при 3000 А. [17]
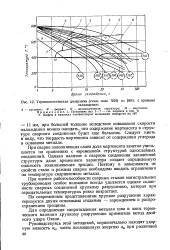 |
Термокинетическая диаграмма ( сталь типа ХЩ из. с кривыми. [18] |
Я - промежуточная структура; М - мартенсит. [19]
А - Промежуточную структуру составляют среднепористые силикагели. [20]
В настоящее время промежуточные структуры часто называют мезомерными, а возможность подобных структур - мсзомерией. [21]
В настоящее время промежуточные структуры часто называют мезомерными, а возможность подобных структур - мезомерисй. [22]
При этом образуется промежуточная структура, как это было названо одним из нас [24], со свободными валентностями. Промежуточная структура не является настоящим промежуточным продуктом, который можно выделить, а лишь схематичным изображением состояния молекулы в момент отнятия элементов воды. [23]
По закономерностям кристаллообразования промежуточных структур, образующихся при нагреве минеральной части угля, намечены схемы химического реагирования основных индивидуальных веществ в золах с силикатной и кальцитной основой. [24]
Какая из этих промежуточных структур преобладает в каждом конкретном случае, можно судить по ряду обстоятельств ( см. стр. В инертном состоянии молекула вероятнее всего приближается к структуре ( I), в то время как остальные три состояния являются активными и присущи молекуле благодаря влиянию на нее среды при химических превращениях. Промежуточные состояния ( 11) и ( III) мы назовем полярными структурами, состояние ( IV) с нелоделенпымн электронами отвечает бирадикалу. Этилену, молекула которого симметрична, присуща только одна полярная структура, в то время как характер полимеризации замощенных этилена или диолсфипов определяется наряду со структурой всей молекулы главным образом характером заместителей при атомах углерода, связанных двойной связью ( см. стр. Исходя из этого этилен следовало бы исключить из системы его замощенных, но, поскольку некоторые реакции его получения аналогичны реакциям получения изобутилена и стирола, а его превращения аналогичны превращениям двух упомянутых мономоров, все три соединения будут рассматриваться в одной главе. [25]
Функции интенсивности для промежуточной структуры потока без ярко выраженной неравномерности структуры располагаются между двумя взаимно перпендикулярными прямыми, соответствующими Л - функциям идеального смешения и вытеснения. Возрастающий характер этих функций объясняется тем, что чем дольше часть жидкости остается в аппарате, тем больше вероятность ее выхода из него. [27]
Образовавшаяся в результате этого промежуточная структура ( V) ароматизируется с одновременным отщеплением протона, который продолжает реакцию. В результате образуется N-катион ( VI), который опять стабилизируется отщеплением протона. Алки-лирование по азоту в данном случае происходит лишь в незначительной степени. [28]
Принцип гибридизации связей допускает дополнительные промежуточные структуры между упомянутыми двумя предельными. Предположение, что добавочные орбиты дегидробензола обладают главным образом р2 - природой со слабым увеличением р-характера, является, по-видимому, правильным. Здесь мы сталкиваемся с новым типом связи, который не соответствует обычной гибридизации. Дженни и Роберте [63], пытаясь объяснить эту необычную связь, предположили, что напряжение в кольце дегидробензола такое же, как в циклопропане. Биполярные структуры, подобные структуре II ( стр. [29]
Тем не менее, циклическая промежуточная структура дает правдоподобное объяснение другим аномальным реакциям. Например, известно, что а р-непределыше альдегиды в противоположность аналогичным кетонам присоединяют гриньяровские реагенты в 1 2-положения, образуя почти исключительно ненасыщенные карбинолы. Эти результаты не являются неожиданными, так как считается, что поляризуемость карбонильной группы и альдегидах выше, чем в кетопах, и, следовательно, альдегидная СО-группа более склонна реагировать быстро, что, по-видимому, благоприятно для 1 2-присоединенпя. Однако, хотя Стивене [47] наблюдал и 1 2-присоедине-ние при взаимодействии кротонового альдегида с гриньяровскими реагентами из бромбензола и бромистых этила, н-пропила и изопро-пила, реагенты из тгерет-бутил - и трет-амилгалогенидов образовывали смеси ненасыщенного карбинола и насыщенного альдегида. К этому следует добавить, что последние гриньяровские реагенты гораздо более реакционноспособны относительно карбонильной группы [48], чем те, которые дали почти исключительно продукты 1 2-присоединения. [30]
Страницы: 1 2 3 4