Теория - переходное состояние
Cтраница 2
Теория переходного состояния допускает, что частицы, столкнувшись, некоторое время ( 10 - u сек) могут находиться вместе; при этом происходят определенные изменения в их строении. Это промежуточное состояние называется активированным состоянием или активированным комплексом; его характеризует величина энергии активации. [16]
Теория переходного состояния позволяет объяснить некоторые особенности реакций в растворах. Так, для ряда мономолекулярных реакций в растворах наблюдаются почти такие же скорости и энергии активации, как и в случае их протекания в газовой фазе. [17]
Теория переходного состояния также делает ясным то обстоятельство, что формальное значение удельной скорости реакции, в которой реагент является подвижной равновесной смесью, определяется формальным значением функции q реагента ( разд. [18]
Теория переходного состояния, строго говоря, применима только для рассмотрения реакций в идеальных газах, когда исходные частицы и активированный комплекс можно рассматривать изолированно от окружающей среды. В растворе образование активированного комплекса из исходных частиц сопровождается теми или иными изменениями молекулярных взаимодействий реагирующих частиц с молекулами растворителя. [19]
Теория переходного состояния имеет важное значение не только для кинетики гомогенных реакций, но и для значительно более широкого круга физико-химических явлений. В частности, она применима для анализа процесса диффузии в твердых телах и жидкостях. [20]
 |
Энтальпийный профиль реакции с образованием интермедиата ( И ( промежуточной частицы. [21] |
Теория переходного состояния применима к реакциям в растворе так же, как в газе. [22]
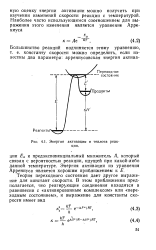 |
Энергия активации и теплота реакции. [23] |
Теория переходного состояния дает другое выражение для констант скорости. [24]
Теория переходного состояния и теория зон предполагают нелинейность зависимости In D f ( l / T) в отличие от экспоненциального уравнения. [25]
Теория переходного состояния представляет собой дальнейшее развитие теории бинарных соударений. Если теория бинарных соударений может объяснить, в некоторых случаях, малые значения величины Р стерическими препятствиями или другими причинами, связанными со строением реагирующих частиц, то наличие нецепных реакций, у которых фактор Р1, совершенно не объяснить этой теорией. [26]
Теория перемей-ного переходного состояния Я2 - реаки. [27]
Теория переходного состояния Герцфельда [196], в которой постулируется существование при сублимации промежуточного слоя, позволяет применить к сублимации понятие активного комплекса. Нейманом [139] постулируется, что при испарении твердых веществ сначала происходит переход молекул в адсорбированный слой и уже затем - в паровую фазу. [28]
Для теории переходного состояния мономолекулярные реакции не представляют собой ничего исключительного, так как для применения методов этой теории безразлично, сколько молекул образует активированный комплекс. [29]
К теории переходного состояния / / Вестн. [30]
Страницы: 1 2 3 4