Энтропийный член
Cтраница 2
Знак энтропийного члена T & S зависит от знака AS, поскольку величина Т всегда положительна. [16]
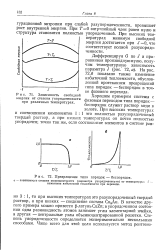 |
Зависимость свободной.| Превращение типа порядок - беспорядок. [17] |
При Т0 энтропийный член равен нулю и структура становится полностью упорядоченной. При высоких температурах минимум свободной энергии достигается при J 0, что соответствует полной разупорядоченности. [18]
 |
Изменение тафелевских наклонов в зависимости от состава сплава. [19] |
Различив в энтропийных членах энергии активации, как предполагают, не зависит от материала электрода. Тогда теплота адсорбции для первой замедленной стадии зависит от прочности связи адсорбированных промежуточных частиц ( разд. [20]
В обоих случаях энтропийный член невелик. Основным параметром, контролирующим процесс, является энтальпийный. [21]
В данном случае энтропийный член не вносит заметного вклада в величину АЯ, поэтому отсутствие его точного значения не может сильно исказить результаты расчета. [22]
 |
Удельная теплоем-кость скол на одну степень. [23] |
К, когда энтропийный член превалирует над энергетическим членом, термодинамически более выгодными оказываются цепочки, поскольку частоты колебательных мод у них ниже, чем у компактных структур. [24]
Небольшое отрицательное значение энтропийного члена объясняется также тем, что маленький по размеру ион Н3О гораздо сильнее способствует ориентации молекул растворителя, чем часто довольно массивный ион RNHa - При диссоциации ионов аммония преобладает, как мы уже указали, тепловой эффект, и поэтому величина рН буферного раствора, содержащего ионы аммония и амины, сильно зависит от температуры. [25]
Первый можно считать энтропийным членом, а второй - энергетическим членом. Когда смешиваются молекулы разного размера, система имеет более высокую энтропию; можно бы ожидать, что это приведет к снижению коэффициента активности. [26]
По крайней мере часть энтропийного члена должна возникать за счет статистических факторов, которые не могут быть, однако, оценены однозначно. [27]
Если рассматривается однокомпонентный кристалл, энтропийный член исчезает и выражение для свободной энергии переходит в уравнение для поверхностной энергии. [28]
Из таблицы видно, что энтропийный член - ГАЗ играет в процессе гидратации значительную роль. Изменение AS гидратации имеет отрицательный знак, что указывает на упорядоченную структуру гидратной оболочки. Однако при набухании и растворении белков изменение свободной энергии превышает изменение энтальпии и энтропия этой системы начинает возрастать. [29]
В дополнение заметим, что энтропийный член Sqi в областях, далеких от критических, имеет положительное начение, поскольку молярная энтропия пара заметно превышает молярную энтропию жидкого гетерогенного комплекса. [30]
Страницы: 1 2 3 4