Электрогидрирование
Cтраница 2
Определенный интерес представляет вопрос о соотношении скоростей процессов каталитического гидрирования и электрогидрирования. Каталитическое гидрирование проводится при пропускании в раствор, в котором находятся электрод-катализатор и гидрируемое органическое вещество, газообразного водорода. Иногда можно встретить утверждение о том, что каталитическое гидрирование и электровосстановление протекают с разными скоростями, так как при каталитическом гидрировании адсорбированный водород образуется при диссоциации молекулярного водорода и в момент образования энергетически отличается от атомарного водорода, возникающего за счет разряда ионов гидрок-сония. Однако убедительные доводы в пользу этого предположения не были получены. [16]
В области спада тока на поляризационной кривой происходит смена медленной стадии электрогидрирования. Это означает, что медленной становится стадия адсорбции молекулы нитрометана. [18]
Работа, связанная с выяснением указанного вопроса, п вообще механизма электрогидрирования с использованием вышеописанных методов, нами продолжается. Интересные данные уже получены при изучении влияния состава и структуры электрода па скорость электрогидрирования, например, показано, что скорость электроглдрирования на смешанном платинопалладиевом электроде примерно в 5 раз больше, чем на чистой платине. [19]
Для построения кинетической кривой адсорбции органического вещества необходимо проведение опытов по электрогидрированию молекул этого вещества, находящихся в адсорбированном 1 состоянии. Потенциал электрода-катализатора доводят до 0 5 - г 0 6 в, вносят органическое вещество, через 15 - 20 минут сливают раствор, промывают несколько раз электролитом и, наполнив окончательно ячейку электролитом, снимают катодную кривую до достижения обратимого водородного потенциала. В данном случае изучалась реакция электрогидрирования в адсорбционном слое органического вещества между молекулами последнего и атомами водорода, которые получаются при разряде ионов гидроксония. [20]
Для построения кинетической кривой адсорбции органического вещества необходимо проведение опытов по электрогидрированию молекул этого вещества, находящихся в адсорбированном состоянии. Потенциал электрода-катализатора доводят до 0 5 - Н 0 6 в, вносят органическое вещество, через 15 - 20 минут сливают раствор, промывают несколько раз электролитом и, наполнив окончательно ячейку электролитом, снимают катодную кривую до достижения обратимого водородного потенциала. В данном случае изучалась реакция электрогидрирования в адсорбционном слое органического вещества между молекулами последнего и атомами водорода, которые получаются при разряде ионов гидроксония. [21]
Процесс каталитической гидрогенизации в присутствии жидкой фазы по своему характеру должен быть ближе к электрогидрированию, чем к гидрированию в газообразной фазе. Присутствие жидкой фазы предопределяет электрохимический характер системы и на границе твердая - жидкая фаза возникает определенный потенциал и двойной электрический слой, влияние которого на процесс восстановления может быть чрезвычайно существенным. Однако гидрирование в присутствии жидкой фазы изучалось каталитиками без учета указанных выше особенностей, и закономерности, установленные при гидрировании в газообразной фазе, распространялись и на процесс гидрирования в жидкой фазе, что не является достаточно обоснованным. [22]
 |
Оптимальные скорости гидрирования в этаноле. [23] |
Это уравнение аналогично уравнению Тафеля и уравнению, выражающему зависимость между Др и W в процессе электрогидрирования. [24]
Давно установлено, что между скоростью реакции на водородном электроде, перенапряжением водорода, каталитической активностью при электрогидрировании органических и неорганических соединений и атомным номером металла имеется периодическая зависимость, обусловленная строением электронных оболочек. [25]
Катодные процессы с участием органических веществ на d - ue - таллах в водных растворах электролитов обычно называют процессами электрогидрирования. [26]
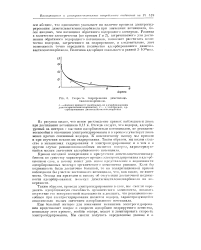 |
Скорость гидрирования дгшетилаце-тиленилкарбипола. [27] |
Еще больший интерес для понимания механизма электроптдрирона-ния представляет вопрос о скорости адсорбции гидрируемого вещостна, поскольку этот процесс, вообще говоря, может и лимитировать скорость электрогидрирования. [28]
Например, при изучении электровосстановления ацетона на платине, иридии и платиново-иридиевых катализаторах ( А. Д. Семенова, Н. В. Кропотова, Г. Д. Вовченко) было обнаружено, что на платине скорости электрогидрирования как хемосорбированного вещества, так и ацетона при присутствии его в растворе близки и приводят к образованию одинаковых продуктов - в основном пропана. В небольших количествах найдены этан и метан, а также изопропиловый спирт. На иридии скорость электрогидрирования прочно хемосорбированного вещества существенно ниже скорости электровосстановления ацетона. Кроме того, из прочно хемосорбированного вещества получается главным образом пропан, тогда как при наличии ацетона в растворе основным продуктом электрогидрирования является изопропиловый спирт. На смешанных платшгово-иридиевых катализаторах с ростом содержания иридия происходит постепенный переход от закономерностей, характерных для платины, к типичным для иридия. [29]
Рассмотренные выше взгляды Вильсона о том, что катоды по своему действию можно разбить на две группы, являются как бы продолжением и развитием работ одного из первых исследователей электрогидрирования органических соединений Фокина [53], который еще в 1906 г. установил, что непредельные соединения лучше восстанавливаются на металлах типа платины и никеля. [30]
Страницы: 1 2 3 4