Давление - пар - насыщенный раствор
Cтраница 4
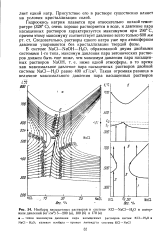 |
Изобары насыщенных растворов в системе КС1 - NaCl - Н2О в интервале давлений ( кГ1смг 5 - 200 ( а, 100 ( б и 170 ( в. [46] |
Гидроокись натрия плавится при относительно низкой температуре ( 328 С), очень хорошо растворяется в воде, и давление пара насыщенных растворов характеризуется максимумом при 290 С, причем этому максимуму соответствует давление всего только 600 мм рт. ст. Сяедовательно, растворы едкого натра уже при атмосферном давлении упариваются без кристаллизации твердой фазы. [47]
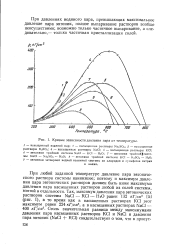 |
Кривые зависимости давления пара от температуры. [48] |
При любой заданной температуре давление пара эвтониче-ского раствора системы наинизшее; поэтому и максимум давления пара эвтонических растворов должен быть ниже максимума давления пара насыщенных растворов любой из солей системы, взятой в отдельности. [49]
Интервал давлений, в котором могут сосуществовать кристаллическая соль и водяной пар, будет наибольшим при температуре / шах, соответствующей максимуму давления пара насыщенных растворов, а затем как при повышении температуры, так и при ее понижении этот интервал будет уменьшаться. Интервал температур, в котором в присутствии водяного пара может существовать кристаллическая соль, по мере возрастания давления будет сужаться и при давлении ргаах, равном максимальному давлению пара насыщенного раствора соли, превращается в нуль. [50]
В литературе имеются данные о растворимости в тройных системах Me SO4 - BeSO - Н2О ( Me1 - щелочной метал л); давление пара насыщенных растворов в этих системах не изучалось. [51]
Результаты исследования растворимости и давления пара в насыщенных растворах галогенидов калия и натрия имели большое значение, так как экспериментально доказали, во-первых, наличие максимума давления пара насыщенных растворов не только в системах из легкоплавких, но и в системах из относительно тугоплав-ских солей и, во-вторых, отсутствие критических явлений в насыщенных растворах во всем температурном интервале их существования даже при температурах, на сотни градусов превышающих критическую температуру воды. [52]
В двух первых системах поля кристаллизация хлоридов и линии совместной кристаллизации хлорида и сульфата исследованы до столь высоких температур ( в некоторых случаях выше 600), что в области кристаллизации хлоридов представилась возможность построить полные диаграммы растворимости и давления пара насыщенных растворов до температур плавления безводных смесей солей. [53]
Температура определялась железо-константановой или хромель-алюмелевой термопарой. Давление пара насыщенных растворов дано с точностью 2 дар. [54]
Температура определялась железо-констан-тановой или хромель-алюмелевой термопарой. Давление пара насыщенных растворов дано с точностью 2 бар. [55]
Как уже отмечалось в главе I, температурный коэффициент растворимости ( ТКР) солей, образующих системы 2-го типа, во всем температурном интервале или начиная с некоторых температур отрицателен, вследствие чего концентрация насыщенных растворов таких солей при температурах, приближающихся к критической температуре воды, становится очень незначительной. Давление пара насыщенных растворов таких солей, в особенности при высоких температурах, близко к давлению пара чистой воды; соответствующие кривые, в отличие от солей 1-го типа, максимума не имеют и заканчиваются в критической точке, параметры которой, вследствие малой растворимости соли, должны быть близки к критическим параметрам чистой воды. [56]
Давление паров над раствором можно представить в виде определенной доли ( или процента) от давления этих паров над чистой жидкостью ( растворителем) при той же температуре. Например, давление паров насыщенного раствора хлористого натрия составляет приблизительно 80 % от давления водяных паров при toft же температуре. Поэтому, если хлористый натрий привести в соприкосновение с воздухом, относительная влажность которого превышает 80 %, то он будет поглощать влагу из воздуха, тогда как при соприкосновении с воздухом меньшей относительной влажности останется сухим. Отсюда вытекает понятие о критической влажности твердой соли: это та влажность, выше которой твердая соль всегда увлажняется и ниже которой всегда остается сухой. [57]
Вследствие непрерывного увеличения растворимости давление пара насыщенных растворов характеризуется наличием максимума. Вначале с повышением температуры давление пара насыщенного раствора повышается, но с ростом температуры возрастает и концентрация насыщенного раствора. В результате борьбы двух факторов - повышения температуры, вызывающего увеличение давления, и повышения концентрации соли, вызывающего уменьшение давления, при дальнейшем возрастании температуры давление пара насыщенного раствора достигает максимума, а затем начинает уменьшаться, доходя до нуля при температуре плавления безводной соли 2, когда содержание воды в растворе также становится равным нулю. [58]
Для построения диаграмм фазовых равновесий могут быть использованы также и все точки, лежащие на ветви кривой, соответствующей насыщенным растворам. Однако эти точки указывают только давления пара насыщенных растворов при тех или иных температурах, но не указывают состав этих растворов. [59]
Кривые показывают, что при данном давлении водяного пара соль существует в кристаллическом состоянии только в некотором температурном интервале, который тем меньше, чем выше давление водяного пара. При давлении водяного пара, равном максимуму давления пара насыщенных растворов, этот интервал становится равным нулю, и в случае более высоких давлений соль уже не может существовать в кристаллическом состоянии ни при каких температурах. Поэтому величина максимального давления пара насыщенных растворов соли является важной характеристикой данной соли, определяющей принципиальную возможность ее существования в кристаллическом состоянии в присутствии водяного пара того или иного давления. [60]
Страницы: 1 2 3 4 5