Копланарность
Cтраница 2
Нарушение копланарности молекулы в результате пространственных препятствий и связанное с этим выключение ориентирующего действия заместителей иногда приводит к весьма интересным, на первый взгляд аномальным, результатам. [16]
Нарушение копланарности аминов ослабляет сопряжение аминогруппы с ядром и повышает основность аминов. [17]
Нарушение копланарности молекулы в результате пространственных препятствий и связанное с этим выключение ориентирующего действия заместителей иногда приводит к весьма интересным, на первый взгляд аномальным, результатам. [18]
 |
Схематическое изображение молекулы диметилксилидина. [19] |
Нарушение копланарности молекулы приводит к отсутствию перекрывания облаков л-электронов и невозможности передачи электронных влияний. Известна, например, высокая реакционная способность пара-положения диметиланилина по отношению к электрофильным реагентам. Если, однако, в орто-положе-нии к диметиламинной группе ввести две метильные группы, то такой диметилксилидин уже не реагирует с азотистой кислотой. [20]
Нарушение копланарности р-электронов гетероатома, участвующих в сопряжении с я-электронами остальной системы, также приводит к изменению в спектрах поглощения. [21]
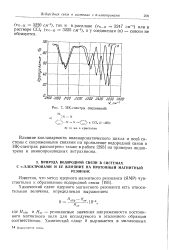 |
ИК-спектры соединений. [22] |
Влияние копланарности квазиароматического цикла и всей системы с сопряженными связями на проявление водородной связи в ИК-спектрах рассмотрено также в работе [293] на примерах индан-трена и аминопроизводных антрахинона. [23]
Приближение к копланарности нарушает оптическую асимметрию у ионизируемого углеродного атома. Поэтому можно ожидать, что в случае протекания реакции с образованием такого карбо-ниевого иона продукт замещения будет рацемизован в той степени, которая будет определяться независимостью этого иона от отщепляющейся замещаемой группы. Экспериментальные факты согласуются с этими соображениями. Если группы R не взаимодействуют ( иначе как через связь С-Я), с положительным центром, образующимся при гетеролитической реакции, то мономолекулярное замещение сопровождается рацемизацией, которая часто протекает в значительной степени. Степень рацемизации зависит от факторов, которые, как этого можно ожидать, определяют устойчивость иона. Например, чем более ионизирован растворитель, тем больше и рацемизация; структурные факторы, благоприятствующие копланарности и способности иона к продолжительному существованию, также оказывают значительное влияние. Это иллюстрируется тем фактом, что emop - иодистые алкилы, претерпевая мономолекулярные замещения, рацемизируются приблизительно на 30 %; в то же время а-фенилэтильные галоидпроизвод-ные, в которых фенильная группа стабилизирует ион в его плоской конфигурации, почти полностью рацемизуются. Та часть продукта, которая не рацемизована, в подобных случаях характеризуется обращенной структурой ( ср. Hughes, Ingold, Martin, Meigh, 1950), поскольку приближающийся нуклеофильный реагент обнаруживает тенденцию отклоняться от соседства с отщепляющейся замещаемой группой. [24]
Сопряжение, копланарность и цвет связаны также со способностью красителей адсорбироваться целлюлозой ( см. гл. [25]
Чаще всего копланарность молекулы нарушается вследствие свободного вращения отдельных частей молекулы вокруг простой С - С-связи. Например, в молекуле бинафтила возможен поворот двух нафталиновых ядер вокруг а-связи С - С, что нарушает сопряжение и-электронов ароматических ядер, поэтому бинафтил - бесцветное соединение. [26]
 |
Плоская модель молекулы дифенила, построенная по правилам, приведенным. [27] |
Вопрос о копланарности подобных молекул решается наличием перекрывания межмолекулярных сфер валентно не связанных атомов. [28]
Сведения о копланарности молекул других дипиридилов отсутствуют, однако, учитывая отличительную особенность строения только 2 2 - ДП, можно предположить, что у 3 3 - и 3 4 - ДП копланарность молекул нарушена в такой же мере, как и у 4 4 - ДП. [29]
 |
Схематическое изображение переходов К-полос в ди-фениле и о-алкилированных дифенилах. [30] |
Страницы: 1 2 3 4