Атом - инертный газ
Cтраница 2
Захвзг атомов инертного газа растущей пленкой, получаемой методом ионного распыления, обсуждается в следующем разделе, вопросы же, относящиеся к росту монокристаллических пленок при ионном распылении, рассматриваются в гл. [16]
Электроны атомов инертного газа находятся в довольно устойчивых состояниях. Поэтому в твердом веществе взаимодействие между атомами оказывается весьма слабым. Волновые функции взаимного перекрытия электронных оболочек имеют низкие значения, а энергетические зоны сравнительно узки. [17]
У атомов инертных газов и некоторых двуатомных молекул ( например, Н2, NJ) дипольные моменты равны нулю. [18]
Валентность атомов инертных газов ( Ne, Аг, Кг, Хе, Rn), имеющих на внешней оболочке восемь электронов, равна нулю, так как в химические реакции с другими элементами они не вступают. К этой же группе относится гелий, имеющий на внешней оболочке два электрона. [19]
Валентность атомов инертных газов ( Ne, Ar, Kr, Xe, Rn), имеющих на внешней оболочке восемь электронов, равна нулю, так как в химические реакции с другими элементами они не вступают. К этой же группе относится гелий, имеющий на внешней оболочке два электрона. [20]
Для атомов инертных газов расчет сил отталкивания довольно прост, но при любом расчете сил отталкивания необходимо учитывать, что эти силы всегда действуют вместе с силами притяжения. Если закон действия сил притяжения хорошо известен, то определение закона сил отталкивания значительно облегчается. Предполагается, что зависимость сил межмолекулярного взаимодействия от расстояния между молекулами не изменяется при переходе вещества из одного агрегатного состояния в другое. [21]
Для атомов инертных газов характерно наличие устойчивых внешних электронных слоев ( у гелия - 2 электрона, у остальных инертных тазов во внешнем слое-8), что обусловливает, как считалось до 1962 года, их исключительную химическую инертность, неспособность давать соединения с ионной и ковалентной связями. [22]
Имитация атомов инертного газа используется Льюисом для объяснения механизма образования ковалентной связи. [23]
Стабильными считаются атомы инертных газов, так как их внешние оболочки полностью заняты. Гелий образует исключение из этого правила. Внешние оболочки атомов других элементов не полностью заняты электронами и соединяются поэтому с атомами того же или другого элемента в молекулы. [24]
Фактически же атомы инертных газов не могут соединяться друг с другом химической ( ковалентной) связью, и их молекулы одноатомны. Однако противоречие с правилом легко устраняется, если вслед за Н. А. Морозовым и А. Е. Ферсманом считать инертные газы главной подгруппой VIII группы. [25]
Итак, атомы инертных газов - от гелия до радона - построены симметрично, их электронные конфигурации предельно замкнуты и максимально прочны. Далее мы убедимся, что такая насыщенность электронной оболочки накладывает неизгладимую печать пе только на химические, но и на многие физические свойства инертных газов. [26]
При плавлении атомы инертных газов образуют жидкости с ближним порядком, соответствующим их гранецентрированным кубическим кристаллическим структурам. [27]
Например, атом инертного газа радона имеет следующую схему строения электронной оболочки ( пор. [28]
Рассмотрим два атома инертных газов. Электронные облака в атомах инертных газов сферически симметричны. Следовательно, эти атомы не имеют постоянных электрических моментов. Поскольку речь идет о статическом распределении зарядов, такие атомы не должны влиять друг на друга. Но опыт и квантовая теория показывают, что частицы не могут находиться в состоянии покоя даже при абсолютном нуле температуры. В процессе движения электронов в отдельные моменты времени распределение зарядов внутри атома может становиться несимметричным. Иначе говоря, в атоме могут возникать виртуальные диполи. Эти очень быстро меняющиеся самопроизвольные или виртуальные диполи создают вокруг атома электрическое поле, которое индуцирует в соседних атомах дипольные моменты. Направление индуцированных моментов всегда таково, что возникает притяжение. Индуцированные диполи находятся во взаимодействии с мгновенными диполями, послужившими причиной их возникновения. [29]
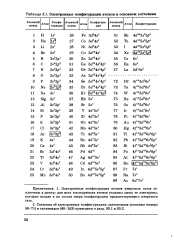 |
Электронные конфигурации атомов в основном состоянии. [30] |
Страницы: 1 2 3 4