Атом - инертный газ
Cтраница 3
Электронные конфигурации атомов инертных газов заключены в рамку; для всех последующих атомов указаны лишь те электроны, которые входят в их состав сверх конфигурации предшествующего инертного газа. [31]
Для возбуждения атомов инертных газов требуются значительные количества энергии, полученные в последние годы оксиды и фториды этих элементов мало устойчивы и представляют собой сильнейшие окислители. [32]
Магнитный момент атомов инертных газов равен нулю, а упругость паров большинства металлов имеет заметную величину только при высоких температурах. Таким образом, доступными для наблюдений объектами являются лишь пары некоторых металлов. Например, для калия в пределах температур 600 ч - 800 С упругость пара составляет 0 5 - - 40 мм рт. ст. Хотя измерения восприимчивости при таких низких давлениях достаточно трудны, они были проведены. [33]
Рассмотрим два атома инертных газов. Электронные облака в атомах инертных газов сферически симметричны. Следовательно, эти атомы не имеют постоянных электрических моментов. Поскольку речь идет о статическом распределении зарядов, такие атомы не должны влиять друг на друга. Но опыт и квантовая теория показывают, что частицы не могут находиться в состоянии покоя даже при абсолютном нуле температуры. В процессе движения электронов в отдельные моменты времени распределение зарядов внутри атома может становиться несимметричным. Иначе говоря, в атоме могут возникать виртуальные диполи. Эти очень быстро меняющиеся самопроизвольные или виртуальные диполи создают вокруг атома электрическое поле, которое индуцирует в соседних атомах дипольные моменты. Направление индуцированных моментов всегда таково, что возникает притяжение. Индуцированные диполи находятся во взаимодействии с мгновенными диполями, послужившими причиной их возникновения. [34]
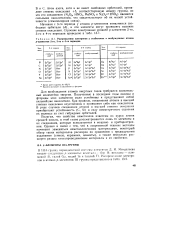 |
Распределение электронов у стабильных и возбужденных атомов р-элементов 2-го, 3-го и 4-го периодов. [35] |
Для возбуждения атомов инертных газов требуются значительные количества энергии. Полученные в последние годы оксиды и фториды этих элементов мало устойчивы и представляют собой сильнейшие окислители. Как правило, соединения атомов в высшей степени окисления неустойчивы и проявляют себя как окислители. В ряде случаев соединения атомов в высшей степени окисления приобретают устойчивость ( С, Si) в силу симметричного строения их молекул за счет гибридных орбиталей. [36]
Для возбуждения атомов инертных газов требуются значительные количества энергии и полученные в последние годы оксиды и фториды этих элементов мало устойчивы и представляют собой сильнейшие окислители. Как правило, соединения атомов в высшей степени окисления не являются устойчивыми и проявляют себя как окислители. В ряде - случаев соединения атомов в высшей степени окисления приобретают устойчивость ( С, Si) в силу симметричного строения их молекул за счет гибридных орбиталей. [37]
ЭПИН-электронная плотность изоэлектронного атома инертного газа; ОС-величина, пропорциональная ЭО атома. Если использовать ковалентные радиусы, то уравнение (2.14) дает ковалентные значения эле -: троотрицательностей атома. Если же в это уравнение подставить ЭПИН и ОС для соответствующих ионов ( метод Сандерсэна позволяет их вычислять из ковалентных значений без привлечения каких-либо геометрических характеристик), то оказалось, что формула Сандерсэна дает размеры ишных радиусов, которые вполне удовлетворительно согласуются с эмпирическими значениями ионных радиусов. [38]
 |
Экспериментальные значения параметров %, Г2 и gp для конфигураций р. [39] |
Особое место занимают атомы инертных газов и редких земель. В первом случае имеет место связь типа jL Как уже отмечалось выше, этот тип связи характерен также для сильно возбужденных состояний ряда других атомов. В случае редких земель ситуация еще окончательно неясна, так как до сих пор для ряда атомов отождествлено и классифицировано очень небольшое число уровней. [40]
Подчеркнем, что атомы инертного газа, как, например, ксенона, могут выступать в этих реакциях в качестве нуклеофилов; уходящей группой могут быть галогеноводороды, вода, нейтральные галогены, боран, а также некоторые другие небольшие нейтральные частицы. [41]
Из-за сферической формы атомов инертных газов можно ожидать, что в твердом состоянии последние будут иметь структуру плотнейшей упаковки; это действительно было обнаружено. Гелий образует плотнейшую гексагональную упаковку, а остальные инертные газы - плотнейшую кубическую упаковку. Чтобы объяснить этот факт, было выполнено большое число теоретических расчетов относительной устойчивости ПКУ и ПГУ. Один из методов расчета предполагает суммирование парных взаимодействий ближайших соседей. Это приближение аналогично тому, которое делают при расчете энергии решетки для ионных кристаллов. В последнем случае определяют взаимодействие одного катиона с одним анионом и затем умножают на геометрический множитель, называемый константой Маделунга. Применив этот метод для кристаллов инертных газов, получили, что ПГУ значительно более стабильна. Однако это находится в противоречии с экспериментальными данными. Более того, нельзя объяснить, исходя из парного взаимодействия сферически симметричных частиц, преобладание ПКУ у инертных газов. Поэтому были предложены два других метода расчета. В первом из них, предложенном Катбертом и Линнетом [2], допускают, что распределение заряда не является сферически симметричным. [42]
 |
Схема образования молекулы хлористого натрия. [43] |
Наконец, у атомов инертных газов, неона и аргона, не способных к присоединению других элементов, внешний слой образован 8 электронами. Очевидно, существует какая-то зависимость между валентностью и числом электронов во внешнем слое. [44]
Если частица М представляет атом инертного газа, то сечения таких процессов па много порядков меньше газокинетичсских. [45]
Страницы: 1 2 3 4