Лиганда - тип
Cтраница 1
 |
Полидентатные хелатные лиганды. [1] |
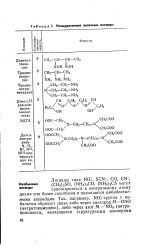
Лиганды типа NO2, SCN -, СО, CN -, ( CHghSO, ( NH2) 2CO, ( NH2) 2CS могут присоединяться к центральному атому двумя или более способами и называются амбидентат ными лигандами. [2]
Трициклические лиганды типа L526 - L532 получили название цилиндрических криптандов. [3]
Поэтому лиганды типа СО называют я-кислотами. Таким образом, карбонилы металлов являются представителями обширного класса комплексов с п-кислотными лигандами. [4]
С лигандами типа цитрата или тартрата, содержащими в качестве связывающих атомов лишь атомы кислорода, цинк образует сравнительно слабые комплексы. Так, наиболее важные в настоящее время реагенты дитизон и ди-р-нафтилтиокарбазон, применяемые для экстракции цинка и его спектрофотометрического определения, образуют с ним внутрикомплексные соединения, связанные через серу и азот. Однако даже эти комплексы диссоциируют и реэкстрагируются из хлороформа и четыреххлористого углерода при встряхивании с разбавленными водными растворами кислот. Комплексообразование с цинконом включает, вероятно, присоединение к металлу двух атомов азота и двух анионных кислоро-дов, что приводит к возникновению тетрадентатного комплекса. В комплексах цинка с 8-оксихинолином и индоксином, по-видимому, образуется дативная связь с ( гетероциклическим) атомом азота. Это менее вероятно при использовании в качестве фотометрического реагента на цинк 1-амино - 2-нафтол - 4-сульфокис-лоты. Цинк также образует экстрагирующиеся комплексы с ди-этилдитиокарбаматом натрия и диэтилдитиокарбаматом диэтил-аммония. [5]
В лигандах типа порфиринов и фталоцианинов большое влияние на прочность комплексов оказывает размер центральной ячейки. Такие крупные ионы, как Hg2 и РЬ2, могут не поместиться в центре порфиринового ядра [12], в то время как для небольших ионов можно ожидать, что устойчивость комплексов будет уменьшаться с уменьшением радиуса катиона, ибо вследствие жесткости порфиринового ядра степень перекрывания ор-биталей иона металла и лиганда будет постепенно падать. Это объяснение прочности комплексов условно: рассмотренные комплексы и другие комплексы, включающие полидентатные лиганды, гораздо более устойчивы, чем комплексы с монодентат-ными лигандами. Этот хелатный эффект частично определяется различиями в изменениях энтропии и частично - гораздо большей энергией, требующейся для разрыва всех связей металла в полидентатных комплексах за время, которое мало по сравнению со временем, необходимым для их образования. В добавление к влиянию на комплексообразование размеров ячейки порфиринов и фталоцианинов геометрия этих лигандов требует плоской квадратной конфигурации их комплексов с металлами. [6]
Таким образом, лиганды типа С2Н4 могут быть донором своей я-пары электронов и акцептором электронной пары металлов на свою разрыхляющую п-орбиталь. [7]
Как правило, лиганды салицилальдиминного типа не выделяются в чистом виде, но все же некоторые исследователи изолировали такие лиганды [6,7] и определили их физические постоянные. Такие соединения обычно получали прямым взаимодействием альдегида и амина в присутствии растворителя или без него. Иногда невозможно получить лиганд прямым взаимодействием. [8]
 |
Типы симметрии молекул III периода Системы. [9] |
Возможность перетягивания р-электронов от лиганд типа F, C1, О к Ga, Ge, As, Se и Вг на пустые 4й - орбитали здесь также уменьшена, как показывают подсчеты, по сравнению с тем, что наблюдалось в третьем ряду Системы. [10]
За исключением комплексов с лигандами я-кислотного типа, молибден и вольфрам имеют мало общего с хромом. Широко представленное у хрома двухвалентное состояние почти не встречается у этих металлов; многочисленные и очень устойчивые комплексы Сг1 практически не имеют аналогов в химии Мо и W. Для этих металлов наиболее характерны высокие состояния окисления, которые отличаются большой устойчивостью и малой склонностью к восстановлению. [11]
Наиболее прочны комплексы с л-акцепторными лигандами CN типа [ 3 ( CN) 4 ] 2 -, которые легко образуются при действии на растворы солей Э ( II) основного цианида. [12]
Наиболее прочны комплексы с л-акцепторными лигандами CN типа [ 3 ( CN) J2 -, которые легко образуются при действии на растворы солей Э ( II) основного цианида. [13]
Первые изученные комплексы А1Вг3 включали лиганды типа эфиров или аминов: А1Вг3 OPh2, А1Вг3 SMe2 и А1Вг3 Ру. В этих молекулярных комплексах угол между эфирной или тиоэфирной плоскостью, определяемой углом С-О - С ( или С-S - С), и осью А1 - О ( Al-S) в различных комплексах неодинаков, что приводит к двум различным конфигурациям. При одной конфигурации два атома брома испытывают более сильное влияние со стороны эфирной молекулы, а при второй конфигурации только один атом брома ( находящийся в плоскости симметрии комплекса) испытывает влияние со стороны тиоэфирной молекулы. [14]
Число изомеров ф с v - лигандами типа /, задается коэффициентом при соответствующем члене полинома в правой части уравнения ( В. [15]
Страницы: 1 2 3 4