Бимолекулярное замещение
Cтраница 3
Вопросы, вставшие перед химиками, изучающими бимолекулярное замещение у ненасыщенного углерода, были следующими: Является ли замещение действительно синхронным. Имеются ли свидетельства в пользу существования стабильного промежуточного соединения. Были получены ответы: Нет - на первый вопрос и, зачастую, Да - на второй. Таким образом, было найдено, что бимолекулярное нуклеофильное замещение при ненасыщенном углеродном атоме по своим основным характеристикам отличается от механизма SN2 при насыщенном атоме углерода. [31]
Эксперимент показывает, что для большинства реакций бимолекулярного замещения характерно ускорение электроноакцепторными заместителями и, таким образом, образование новой связи обгоняет разрыв старой. [32]
Подобный механизм обращения конфигурации является общим для любого бимолекулярного замещения, но, разумеется, его можно обнаружить по изменению направления вращения плоскости поляризации света только в случае оптически деятельных соединений. [33]
Как мы видели при рассмотрении реакций Зн2, бимолекулярное замещение весьма чувствительно к стерическим эффектам. Так как при отрыве протона, находящегося на периферии молекулы, стерические препятствия играют значительно меньшую роль, чем при взаимодействии с атомом углерода в реакции замещения, увеличение стерического объема нуклеофила способствует реакциям отщепления. Использование нуклеофилов с большим объемом ( например, этилдиизопропиламина) может привести к тому, что реакция отщепления станет единственным процессом. [34]
Эти результаты наводят на мысль о возможности механизма бимолекулярного замещения с ароматическими углеводородами, ведущими себя как нуклеофильный замещающий агент. [35]
Быстрая скорость обмена для квадратно-плоскостных соединений обусловлена низкоэнергетическим маршрутом бимолекулярного замещения. Медленный обмен для C5H5Fe ( CO) 2X предполагает, что эти соединения обладают скорее свойствами систем с КЧ 6, чем свойствами искаженного тетраэдра, принципиально возможного в этом случае. [36]
Уменьшение специфической сольватации нуклеофила является главной причиной ускорения реакций бимолекулярного замещения типа анион - молекула в апротонных биполярных растворителях. [37]
Эти нуклеофильные реагенты вызывают реакцию элиминирования ( наряду с бимолекулярным замещением) в значительно большей степени, чем этого можно было ожидать ввиду их слабой основности. [38]
Далее будет допущено, что она может реализоваться в бимолекулярном замещении у кобальта молекулярным реагентом. [39]
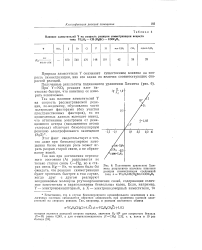 |
Подчинение уравнению Хаммета результатов изучения кинетики реакции симметризации соединений типа n YC6H4CH ( HgBr COOC2H6. [40] |
Этот факт свидетельствует о том, что даже при бимолекулярном замещении более важную роль может играть разрыв старой связи, а не образование новой. [41]
 |
Геометрия бимолекулярного переходного состояния при октаэдрическом замещении без перемещения по ребру ( I и с перемещением по ребру ( II. [42] |
Далее будет допущено, что она может реализоваться в бимолекулярном замещении у кобальта молекулярным реагентом. [43]
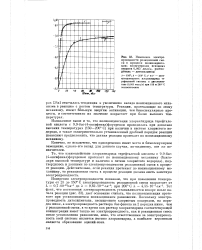 |
Изменение электропроводности реакционной смеси в процессе поликонденсации. концентрации исходных веществ 0 065 молъ / л, растворитель - дитолилметан. [44] |
Конечно, не исключено, что одновременно имеет место и бимолекулярное замещение, однако его вклад для данного случая, по-видимому, все же незначителен. [45]
Страницы: 1 2 3 4