Заряд - ион - металл
Cтраница 2
Один из активных компонентов смеси должен обладать способностью нейтрализовать заряд экстрагируемого иона металла. Это имеет место предпочтительно при образовании внутрикомплексного соединения или хелата вообще. [16]
Если координационное число иона металла относительно реагента больше, чем заряд иона металла, образуются анионные комплексы, обычно растворимые в воде. Такие комплексы образуются при маскировании, например растворимые комплексы металлов с оксалатом, цитратом и тартратом. [17]
Стабильность адсорбированных комплексов н а - центрах Льюиса зависит от величины заряда иона металла в катализаторе и от радиуса этого иона. Известно, что на скорости отдельных реакций, протекающих с участием кислот и оснований, значительно влияют сила этих кислот и оснований и число кислотных и основных центров на поверхности. [19]
Хотя теноилтрифторацетон ( ТТА) наиболее широко используется как хелатирующий реагент для нейтрализации заряда иона металла, было найдено, что его заменителями являются и другие ( 3-дикетоны, а также некоторые азотсодержащие хелатирующие агенты ( купфе-роп, диметилглиоксим и 8-оксихйнолин), нельзя применять фосфор-органические эфиры. Нейтральными компонентами могут быть спирты, кетоны, амины. Степень синергетического увеличения ( в общем случае порядка 108) зависит главным образом от природы и свойств нейтрального компонента. [20]
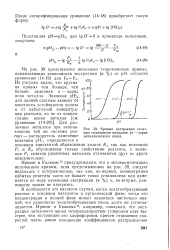 |
Кривые экстракции хелат-ных комплексов металлов, ( п - заряд металлического иона. [21] |
Из рисунка видно, что крутизна кривых тем больше, чем больше величина п - заряд иона металла. [22]
Лиганды третьего типа имеют две анионных группы ( например, щавелевая кислота), и заряд иона металла уменьшается на две единицы после хелатообразования с одной молекулой лиганда. [23]
Следовательно, эквивалент основания может быть вычислен как частное от деления молекулярной массы основания на заряд иона металла или, что то же самое, на кислотность основания. По тем же соображениям эквивалент соли может быть вычислен как частное от деления ее молекулярной массы на произведение числа ионов металла и его заряда. [24]
Лиганды третьего типа имеют две анионных группы ( например, щавелевая кислота), и заряд иона металла умень шается на две единицы после хелатообразования с одной молекулой лиганда. [25]
Это является следствием наличия у молекул воды определенного дипольного момента, благодаря чему под влиянием заряда иона металла происходит их пространственная ориентация. [26]
В этой формуле е0 - нормальный потенциал металла ( по табл. 39), п - заряд иона металла ( его валентность) и С, - концентрация этих ионов в растворе в г-ыон / л ( C ( Cdfe - стр. [27]
 |
Схема трансвлияния по Некрасову. [28] |
Если в плоскоквадратном комплексе все четыре ли-ганда одинаковы, то в каждом из них под действием заряда иона металла индуцируется одинаковый диполь. Это приводит к дополнительному, неравному закреплению всех лигандов. В таком случае в центральном атоме результирующие диполь ле возникает, и поле его остается изотропным. При замене одного лиганда на другой, ( рис. 8.3) в центральном атоме. X и Y по своим поляризационным свойствам и чем легче деформируется центральный атом. Например, еслиТЭаИйЕная: поляризация Y и центрального атома больше, чем центрального атома и X, то диполь направлен так, как показано на рис. 8.3, б; если она меньше - в противоположную сторону. Поэтому поле центрального атома становится анизотропным что, в свою очередь, сказывается на прочн ости связл отдельных лигандов с металлом. Так, оба лиганда X, расположенные в 1 И. [29]
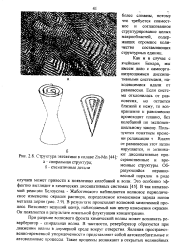 |
Структура эвтектики в сплаве Zn-Mn. [30] |
Страницы: 1 2 3 4