Низкий заряд
Cтраница 2
 |
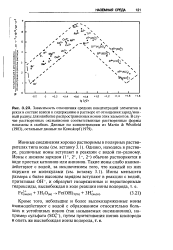
Расположение элементов класса Б в Периодической системе элементов Д. И. Менделеева. [16] |
Если устойчивость комплекса существенно зависит от образования дативной связи, ей благоприятствуют низкий заряд и большая поляризуемость центрального иона. Низкий заряд увеличивает число электронов у центрального атома и усиливает его я-до-норный характер. Поэтому, например, ион Си относится к классу Б, а Си2 нет. [17]
В отличие от катионов класса А здесь устойчивости комплексов благоприятствуют низкий заряд и большая поляризуемость центрального иона. Низкий заряд увеличивает число электронов у центрального атома и менее препятствует образованию дативной связи. Поэтому, например, ион Си относится к классу Б, а Си2 нет. [18]
Окислительно-восстановительные равновесия в растворах солей Cu ( I) и ( II) осложняются легкостью диспропорционирования Cu ( I) в Си ( 0) и Си ( II), поэтому комплексы Си ( 1) обычно образуются только в том случае, если они нерастворимы ( например, CuCN и Cul) или если связь металл-лиганд имеет главным образом ковалентный характер, а пространственные факторы благоприятны. Низкий заряд Си и его 3 10-электронная структура приводят к тому, что Cu ( I) образует наиболее прочные комплексы с сильнополяризующимися лигандами, особенно в тех случаях, когда возможно обратное двойное связывание. К известным примерам, используемым в фотометрических методах, относятся производные а, а - дипиридила и 1 10-фенантролина. [19]
Однако, находясь в растворе, различные ионы вступают в реакции с водой по-разному. Ионы с низким зарядом ( 1, 2, 1 -, 2 -) обычно растворяются в виде простых катионов или анионов. [21]
Большое изменение энтропии возникает главным образом оттого, что каждый заряженный реактант имеет упорядоченную сольватную оболочку. Продукты реакции, имеющие более низкий заряд, сольватированы значительно меньше. [22]
Соли щелочных металлов и их гидроокиси в водном растворе не только полностью диссоциированы, но и силы взаимного притяжения свободных ионов там также сравнительно незначительны. Это обусловлено, во-первых, низким зарядом, но, кроме того, большими ионными радиусами. Влияние последних становится особенно заметным в концентрированных растворах. [23]
Соли щелочных металлов и их гидроокиси в водном растворе не только полностью диссоциированы, но и силы взаимного притяжения свободных ионов там также сравнительно незначительны. Это обусловлено, во-первых, низким зарядом, но, кроме того, большими лонными радиусами. Влияние последних становится особенно заметным в концентрированных растворах. [24]
Соли щелочных металлов и их гидроокиси в водном растворе не только полностью диссоциированы, но и силы взаимного притяжения свободных ионов там также сравнительно незначительны. Это обусловлено, во-первых, низким зарядом, но, кроме того, боль-щими ионными радиусами. Влияние последних становится особенно заметным в концентрированных растворах. [25]
Первая группа параметров, отраженная в табл. 4.7, показывает, что для стеклообразующих катионов типичны высокие заряды ионов, малые значения ионных радиусов и координационных чисел, и, как следствие, высокая напряженность поля. Для элементов-модификаторов, напротив, характерны низкие заряды ионов, большие ионные радиусы и координационные числа в сочетании с низкой напряженностью поля. Для стеклообразующих оксидов характерны высокие значения прочности химической связи. [26]
Строение и химические свойства упомянутых выше веществ не описаны. Сравнительная устойчивость их может быть объяснена низким зарядом катиона. [27]
Представьте, что поганый забрался в наше общее сознание. Он ползает по нему, находит точки с высоким и низким зарядом и закорачивает их. Ему абсолютно все равно, какие это точки, его цель - просто замкнуть, омертвить. Поганый сидит, смотрит на искры, радуется, улюлюкает, слюной исходит. [28]
Известны перхлораты практически всех электроположительных металлов. За исключением некоторых из них, образованных большим катионом с низким зарядом ( CsClO4, RbClO4 и КСЮ4), все они легко растворимы в воде. Твердые перхлораты с тетраэдричес-ким перхлорат-ионом часто изоморфны перманганатам, сульфатам, фтороборатам и другим солям с тетраэдрическими анионами. Особо важным свойством перхлорат-нона является очень слабая склонность его быть лигандом в комплексных соединениях, поэтому перхлорат часто используют при изучении комплексообразования в предположении, что поправка на концентрацию перхлоратного комплекса незначительна. Хотя это может быть справедливо для водных и очень похожих на них растворов, недавно появились сообщения о том, что если других конкурирующих доноров нет, то перхлорат-ион проявляет докорную емкость. Возможно, соединения ПО ] ( CH3) oSnClO4 и [ Со ( MeSC. [29]
Известны перхлораты практически всех электроположительных металлов. За исключением некоторых из них, образованных большим катионом с низким зарядом ( CsClO4, RbClO4 и КС1О4), все они легко растворимы в воде. Твердые перхлораты с тетраэдричес-ким перхлорат-ионом часто изоморфны перманганатам, сульфатам, фтороборатам и другим солям с тетраэдрическими анионами. Особо важным свойством перхлорат-иона является очень слабая склонность его быть лигандом в комплексных соединениях, поэтому перхлорат часто используют при изучении комплексообразования в предположении, что поправка на концентрацию перхлоратного комплекса незначительна. Хотя это может быть справедливо для водных и очень похожих на них растворов, недавно появились сообщения о том, что если других конкурирующих доноров нет, то перхлорат-ион проявляет донорную емкость. Возможно, соединения [ 101 ( CH3) 3SnClO4 и [ Со ( MeSC2H4SMe) 2 ( C1O4) 2 ] являются наиболее яркими примерами этого. [30]
Страницы: 1 2 3 4