Анион - иод
Cтраница 1
Анионы иода как восстановитель реагируют со свободными галогенами ( С12 и Вг2), с Н2О2, KMnO4, K2Cr2Oi и с другими окислителями, которые окисляют их до свободного иода. [1]
Значительно большая поляризуемость аниона иода по сравнению с этилат-ионом приводит, кроме того, и к меньшей чувствительности аниона иода к стерическим препятствиям в субстрате. Поэтому при переходе от этилбромида к неопентилбромиду замедление скорости взаимодействия с иодид-ионом должно происходить в меньшей степени, чем при использовании этилат-иона. [2]
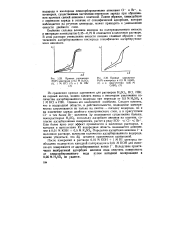 |
Кривые заряжения.| Кривые заряжения. [3] |
Вследствие практически необратимой адсорбции анионов иода очистить поверхность от хемосорбированного иода путем катодной поляризации в 0 Q5MHjSO4 не удается. [4]
К одноэлектронному переносу способен только анион иода. [5]
Появление желтой окраски из-за окисления аниона иода ионом трехвалентного железа исключается, благодаря применению муравьиной кислоты. Но желтая окраска может появиться вследствие образования соединения хинина или цинхонина с иодидом. Поэтому при выполнении анализа нужно брать минимальное количество сульфата хинина. [6]
При этом иод восстанавливается до аниона иода, а анион серноватистой кислоты окисляется в анион тетратионовой кислоты. В результате бурый раствор иода обесцвечивается. [7]
Окраска возникает вследствие переноса заряда с аниона иода на нижнюю я-разрыхляющую МО катиона, подтверждением чего служит хорошая корреляция положения длинноволновой полосы поглощения солей с потенциалами их полярографического восстановления. [8]
Таким образом, в условиях катализа анионом иода имеет место двойное обращение. [9]
Известно также, что процесс растворения никеля тормозится в присутетвии анионов иода. Это явление объясняется торможением процесса адсорбции ионов 80 вследствие их взаимодействия с га - лоидными ионами. [10]
Из таблицы видно, что энергии водородных связей ОН-грушг воды с анионом иода или протоно-акцепторным органическим растворителем существенно зависят от природы катиона. [11]
При определении таллия в иодиде натрия следует иметь в виду, что анион иода с родамином С образует комплекс, который извлекается бензолом, при этом наблюдается флуоресценция экстракта. Для удаления иода были применены273 последовательно ряд операций: основную массу иода удаляли путем двухкратного кислотного разложения иодида натрия серной кислотой с прокаливанием и плавлением соли. [12]
Объяснение [24] этого факта основано на предположении, что органический катион и анион иода образуют донорно-акцепторный комплекс, в спектре которого имеется полоса поглощения переноса заряда. [13]
В большинстве случаев поляризующее влияние катиона и поляризуемость анионов ( особенно таких, как анион иода, серы, кислорода) приводят к увеличению ковалентного характера связей. Другим фактором, оказывающим действие на состояние связей, является степень экранирования катиона соединенными с ним анионами. Решетка хлорида алюминия, возникшая при конденсации газообразного хлорида, имеет все шансы сохранить в узлах молекулы - ее ионный характер выражен очень слабо. Но уже фторид алюминия, в молекуле которого ион алюминия окружен анионами меньшего радиуса, дает при конденсации решетку ионного типа и само соединение имеет солеоб-разный характер. [14]
Свободный иод даже в самых незначительных концентрациях с раствором крахмала дает синюю окраску, тогда как анион иода с крахмалом не дает окраски. На этом основано применение в иодометрии крахмального раствора в качестве индикатора. [15]
Страницы: 1 2 3 4