Активация - химическая реакция
Cтраница 4
Увеличение содержания геля при повышении температуры переработки еще раз подчеркивает роль процессов активации химических реакций механическими напряжениями, не связанных с процессом механической деструкции макромолекул, эффективность которого с повышением температуры снижается. [46]
Этот параметр интересен тем, что он связывает величину перегрева с энергией активации химической реакции. При небольших значениях перепрев незначителен, при больших значениях ( десятки единиц) возможен заметный перегрев. [47]
Получаемые при использовании методики работы в адсорбированном слое результаты - истинная энергия активации химической реакции непосредственно на активных участках, число этих участков, характер их распределения и пр. [49]
Теплота адсорбции нередко бывает очень значительной, и когда она больше истинной энергии активации химической реакции, скорость может даже падать с повышением температуры. [50]
Приводимые в статье примеры показывают, что электрические разряды представляют собою мощное средство активации химических реакций, в равной степени пригодное как для теоретических исследований в лабораториях, так и для осуществления химических процессов в промышленности. [51]
Как известно, методы современной квантовой химии не позволяют теоретически вычислять абсолютные значения энергии активации химических реакций с точностью, которая была бы достаточна для решения вопросов кинетики и механизма химических реакций. Однако квантовая химия, используя идею о пере ч) дном состоянии реакции, позволяет теоретически обсудить вопрос о влиянии различных факторов на величину энергии активации в ряду однотипных реакций. Несколько лет назад автором [ 2, 4j был предложен другой метод рассмотрения этого вопроса. [52]
 |
Энергия активации А ( кДж / моль для некоторых реакций. [53] |
Определим увеличение скорости химической реакции при повышении температуры, если, например, энергия активации химической реакции А 166 200 Дж / моль, а температура изменяется от 500 до 600 С. [54]
Теория ВС чрезвычайно удобна для объяснения насыщаемости химической связи, направленной валентности, энергии активации химических реакций и др. Однако оказалось невозможным использовать эту теорию для количественного описания строения соединений с сопряженными связями, с нечетным числом электронов ( например, молекулярные радикалы), а также для расчета количественных значений молекулярных характеристик и строгого описания спектров молекул. [55]
Определим увеличение скорости химической реакции при повышении температуры, если, например, энергия активации химической реакции А - 166 200 Дж / моль, а изменение температуры - от 600 до 600 С. [56]
Скорость газовыделения в этом случае определяется скоростью химической реакции, а энергия активации соответствует энергии активации химической реакции. При скоростном нагреве прогрев частиц материала зависит от их размера, разницы температур тела и источника тепла, теплопроводности материала и расхода тепла на реакции его разложения. [57]
 |
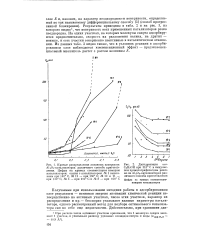
Зависимость скорости образования гидроперекиси изопропилбензола от ее концентрации в реакционной массе и температуры при Р0 0 135 кгс / см2. [58] |
С также определяют с помощью экспериментальной кривой для какой-либо одной температуры, а величину энергии активации химической реакции Е находят прямыми измерениями в кинетической области ведения процесса. [59]
Мы говорили также что переходу в кинетическую область способствует понижение температуры, так как энергия активации химической реакции больше энергии активации процесса диффузии. Другими словами, чем выше температура, тем быстрее сама реакция и тем большее перемешивание требуется, чтобы остаться в кинетической области. [60]
Страницы: 1 2 3 4 5