Активирование - молекула
Cтраница 2
Траубе установил, что при самоокислении цинка в присутствии воды и воздуха до окиси цинка и перекиси водорода не происходит активирование кисло родной молекулы, так как при этом такие легко окисляемые вещества, как индиго-сульфокислота, не окисляются. Таким; образом, перекись водорода является не высшей степенью окисления воды, как это предполагалось до Траубе, а, наоборот, - продуктом восстановления кислорода. [16]
Образование непрочных ионизированных комплексов за счет протона и кислородного атома вещества или возникновение молекулярных соединений кислоты с исходным веществом, а также и с продуктами реакции, приводят к активированию молекул и вызывают изомеризацию, что сопровождается изменением в расположении и соотношениях электронов. [17]
Из немногочисленных попыток осуществить синтетический абсолютный асимметрический синтез следует указать на неудачные опыты Шер-булье [20] - бромирование замещенной коричной кислоты при воздействии циркулярно-поляризованного света; однако действие радиации заключалось только в активировании молекул брома, что не могло, конечно, повлечь за собой асимметрической реакции. Ошибка была допущена и в работе Падоа [29], бромировавшего ангеликовую кислоту при воздействии циркулярно-поляризованного света. В 1922 г. Пирак [30] в тех же условиях безуспешно пытался получить оптически активный продукт присоединения синильной кислоты к ацетальдегиду. [18]
Поскольку скорость мономолекулярных реакций пропорциональна первой степени давления или концентрации, постольку первые попытки объяснить мономолекулярные реакции сводились к поискам механизма активации без учета молекулярных столкновений ( в результате которых в бимолекулярных реакциях происходит активирование молекул), а за счет какого-то другого процесса. Например, было сделано предположение, что активация происходит вследствие поглощения инфракрасного излучения ( фотохимический процесс), передачи необходимой энергии молекулам возбужденными частицами продуктов реакции и др. Такие предположения не получили экспериментального подтверждения. Более достоверное объяснение механизма мономолекулярных реакций предложил в 1922 г. Линдеман, применивший гипотезу о столкновении молекул. Он исходил из предположения, что данная молекула А распадается только тогда, когда она обладает колебательной энергией, достаточной для разрыва связей между атомами или атомными группами. [19]
 |
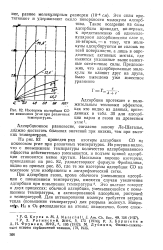
Влияние температуры на скорость образования ( w продуктов взаимодействия пропилена с фенолом ( а и трег-бутиловым спиртом - ( б. [20] |
Промотирующее действие добавок связывают с тем, что они, способствуя образованию поверхностного ацетата путем отщепления атома водорода от карбоксильной группы уксусной кислоты, повышают степень адсорбции кислоты на твердой поверхности. Активирование молекулы олефина происходит вследствие образования промежуточного1 продукта его дегидрирования. [21]
 |
Изотермы адсорбции СО. [22] |
Это явление говорит о двух процессах: обычной адсорбции, уменьшающейся с повышением температуры, и активированной адсорбции, растущей с температурой. Для активирования молекул требуется затрата тепла ( повышение температуры) для разрыва молекул. [23]
ЗО схематически показан механизм образования связи атома металла с молекулой азота. Он предусматривает активирование молекулы N2 и затем ее связывание в мягких условиях. Аналогичным образом объясняется действие соединений d - элементов как катализаторов в процессах синтеза аммиака или при связывании азота микроорганизмами. Сначала происходит образование донорно-акцепторной связи a - типа. Это требует переноса электронной плотности за счет перекрывания занятой орбитали атома азота ( свободная пара электронов) с незанятой орбиталью атома металла. [24]
 |
Цикл трикарбоповых кислот. Стрелками показано направлепие, а номерами - иорядок реакций. [25] |
Заключительная реакция дыхания - это присоединение протона и электрона к кислороду воздуха и образование воды. Но прежде происходит активирование молекулы кислорода под действием фермента ц и т о-хромоксидазы. Активирование сводится к тому, что кислород приобретает отрицательный заряд за счет присоединения электрона окисляемого вещества. К активированному кислороду присоединяется водород ( протон), образуя воду. [26]
Первое из них допускало активирование молекулы в результате разрыва ее на активные половины. Траубе [21], впервые допустивший, что активирование кислорода может происходить в результате разрыва лишь одной связи в его молекуле. [27]
От давления ( концентрации) порядок не зависит, и реакция является настоящей бимолекулярной реакцией. Определяющей стадией процесса здесь является активирование молекул посредством бинарных соударений. [28]
Недостатком описанного выше способа получения полиэтилена является необходимость использования сложного компрессорного хозяйства для создания весьма высоких давлений. Только сравнительно недавно найден путь для активирования молекул этилена с помощью катализаторов, который открыл возможность получения высокомолекулярного полиэтилена при низком и даже атмосферном давлении. [29]
Чтобы определить количество активных столкновений, необходимо знать энергию активации молекул. Элементарный химический акт состоит из трех стадий: активирование молекул путем столкновения двух частиц; химическое превращение активных молекул и дезактивирование активной молекулы путем отдачи ею части энергии неактивной молекуле. Последнее также осуществляется при бинарном соударении активных и неактивных молекул. [30]
Страницы: 1 2 3 4