Активность - ион - хлор
Cтраница 2
Равновесие в полуэлементе зависит от равновесия этой реакции, определяющей активность ионов хлора в растворе. Газовые электроды применяют в топливных элементах ( стр. [16]
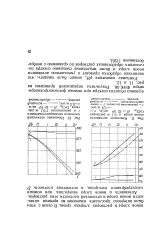 |
Изменение активности ионов хлора в 0 1 т растворах СгС13, Н - 12 104 ав / м, v.| Изменение оптической плотности свежеприготовленного / и равновесного 2 0 1 от раствора СгС13, Я 12 - 10 ав / м. [17] |
В связи с этим было интересно проследить изменение во времени активности ионов хлора и оптической плотности этих растворов. [18]
 |
Потенциал каломельного электрода.| Хлорсе-ребряный электрод. [19] |
В насыщенном растворе каломели в присутствии хлорида калия активность ионов ртути определяется активностью ионов хлора. [20]
Опыты [192] показали, что в цементе с содержанием С3А 8 - 10 % активность ионов хлора в процессе твердения быстро падает. При отсутствии СзА, наоборот, активность хлор-ионов возрастает в результате связывания воды в процессе схватывания. Наличие в цементе сульфатов также тормозит связывание ионов хлора, так как в первую очередь алюминаты расходуются на образование гидросульфоалюмината кальция. [21]
Из уравнений ( VII43) и ( VII42) видно, что при увеличении активности ионов хлора С1 - или при уменьшении активности ионов ртути Hgi потенциал каломельного электрода становится более отрицательным. Активность ионов хлора С1 -, а значит и ионов Hgl зависит от концентрации хлористого калия в растворе. Обычно, пользуются растворами трех концентраций хлористого калия: 0 1; 1 0 кн. и насыщенным. [22]
Несмотря на то что проводимость раствора хлоридов алюминия довольно высока, можно показать, что активность ионов хлора в растворе приблизительно соответствует активности чистого растворителя. Раствор хлорида алюминия в оксихлориде фосфора находится приблизительно в изоэлектрической точке, как это, например, имеет место у гидроокиси алюминия в воде. [23]
 |
Конструкция хлорсерсбряного электрода. [24] |
Одна из распространенных форм хлор-серебряного электрода представлена на рис. 6.4. Потенциал такого электрода зависит только от активности ионов хлора в растворе. [25]
Этот прием дает возможность определить рйН с такой точностью, с какой возможна оценка величины коэффициентов активности иона хлора. [26]
Сс - - концентрация ионов хлора, г-ион / л; / ci - - коэффициент активности ионов хлора. [27]
Этот прием дает возможность определить раН с такой точностью, с какой возможна оценка величины коэффициентов активности иона хлора. [28]
Оказалось, что в соответствии с требованиями теории, логарифм коэффициента распределения линейно растет с увеличением логарифма активности иона хлора в водной фазе. [29]
В; Cci - - концентрация ионов хлора, ион / л; fci - - коэффициент активности ионов хлора. [30]
Страницы: 1 2 3 4