Алкилгалоге-нид
Cтраница 1
Алкилгалоге-нид встряхивают с 500 мл воды. Водную вытяжку, очищенную от органических соединений встряхиванием с небольшим количеством эфира, обрабатывают затем нитратом серебра. Осадок бромистого - Br80 серебра собирают, промывают спиртом и быстро сушат. [1]
Легче всего реагируют первичные алкилгалоге-ниды, труднее-вторичные; третичные ( кроме Аг3СНа1) совсем не реагируют. [2]
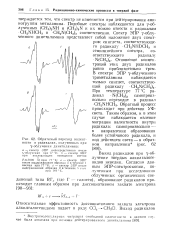 |
Обратимый переход валентности в радикалах, полученных при. [3] |
Выход радикалов при у-об-лучении твердых алкилгалоге-нидов невелик. [4]
Для получения простых эфиров вместо алкилгалоге-нидов можно использовать энергичные алкилирующие средства - диалкилсульфаты или толуолсульфонаты. [5]
 |
УФ-Спектры полисульфидных олигомеров, полученных на основе 2 2 -ди-хлордиэтилформаля ( а и 2 2 - ди ( хлорэти. чэтокси фор-маля ( б. [6] |
Однако полисульфидные олигомеры на основе алкилгалоге-нидов трудно использовать на практике из-за их большой склонности к кристаллизации, а олигомеры, содержащие бутиленок-сидные и бутиленформалевые звенья, трудно синтезируются. Поэтому на практике для синтеза полисульфидных олигомеров всегда используется 2 2 -дихлордиэтилформаль или его смеси с дру - ими мономерами, например с 2 2 -дихлордиэтиловым эфиром или 1 2-дихлорэтаном. [7]
В результате взаимодействия алкилбензола с алкилгалоге-нидом [ уравнение (5.1) ] в качестве побочного продукта образуется галогеноводород, который может протонировать образовавшийся диалкилбензол, основность которого выше, чем у бензола и алкилбензола. [8]
В результате взаимодействия элкилбензола с алкилгалоге-нидом [ уравнение (5.1) ] в качестве побочного продукта образуется галогеноводород, который может протонировать образовавшийся диалкилбензол, основность которого выше, чем у бензола и алкнлбензола. [9]
Хорошо известна реакция превращения спиртов в алкилгалоге-ниды под действием галогенфосфоранов; при более высоких температурах эта реакция может использоваться также для получения арилгалогенидов из фенолов. [10]
Особенно легко по этой схеме реагируют третичные алкилгалоге-ниды, аллил - и бензилгалогениды. [11]
Особенно легко по этой схеме реагируют третичные алкилгалоге-ниды, аллил - и бензилгалогениды. [12]
Большое число соединений Гриньяра и ряд других алкилгалоге-нидов металла и металлалкилы склонны к обмену своего алкильного остатка на галоген, а также на кислород или азотсодержащую группу. Этот вид реакций позволяет получать алкил - или арилсоединения многочисленных других элементов. [13]
Этот тип деструкции обычен для алкилацетатов, алкилгалоге-нидов. Однако в случае довольно нестабильных полиэфиров метакриловой кислоты по такому закону разрушаются лишь полимеры на основе эфиров третичных спиртов. Остальные в результате их нестабильности деполимеризуются по цепному механизму с образованием мономера. [14]
Арилгалогениды проявляют гораздо меньшую реакционную способность, чем алкилгалоге-ниды. Для протекания реакции замещения в этом случае требуется длительное нагревание в присутствии меди. Арилирова-ние аммиака приводит к образованию первичных ариламинов. Реакция облегчается при наличии акцепторных групп в орто-и ( или) пара-положениях [ О. [15]
Страницы: 1 2 3 4